
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅤⅡA | 0 |
| 2 | C | N | O | |||||
| 3 | Na | Mg | Si | S | Cl | Ar | ||
| 4 | Ca |
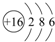 ;其最外层共有6种不同运动状态的电子;
;其最外层共有6种不同运动状态的电子;分析 (1)S原子核外电子数为16,有3个电子层,各层电子数为2、8、6;核外没有运动状态相同的电子;
(2)同周期自左而右金属性减弱,根据根据金属与水的反应剧烈程度判断;
(3)非金属性越强,最高价氧化物对应水化物的酸性越强,氢化物越稳定;
(4)同周期自左而右原子半径减小;
(4)硅的氧化物为为二氧化硅,属于共价化合物,常用于制造光导纤维等.
解答 解:(1)S原子核外电子数为16,有3个电子层,各层电子数为2、8、6,原子结构示意图为 ,最外层有6个电子,最外层共有6种不同运动状态的电子,
,最外层有6个电子,最外层共有6种不同运动状态的电子,
故答案为: ;6;
;6;
(2)同周期自左而右金属性减弱,故金属性Na>Mg,Na与水反应剧烈,Mg与水反应现象不明显,说明金属性Na>Mg,
故答案为:Na;Na与水反应剧烈,Mg与水反应现象不明显;
(3)第三周期中Cl元素非金属性最强,故最高价氧化物对应水化物的酸性最强的为HClO4,HCl最稳定,
故答案为:HClO4;HCl;
(4)同周期自左而右原子半径减小,故原子半径O<N<C,
故答案为:O<N<C;
(4)硅的氧化物为为二氧化硅,属于共价化合物,常用于制造光导纤维等,
故答案为:共价;光导纤维.
点评 本题考查元素周期律、原子结构示意图、元素化合物知识等,比较基础,注意掌握金属性、非金属性强弱比较实验事实.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
| A元素的核外电子数和电子层数相等 |
| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能如下: I1=738kJ•mol-1 I2=1451kJ•mol-1 I3=7733kJ•mol-1 I4=10540kJ•mol-1 |
| D原子价电子层的p轨道半满 |
| E元素的主族序数与周期数的差为4 |
| F是前四周期中电负性最小的元素 |
| G在周期表的第七列 |
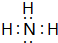 .
.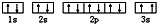 ,该同学所画的电子排布图违背了泡利原理.
,该同学所画的电子排布图违背了泡利原理.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 酸 | 电离常数 |
| 碳酸 | K1=4×10-7 K2=5.6×10-11 |
| 亚硫酸 | K1=1.54×10-2K2=1.02×10-7 |
| A. | SO2+H2O+2CO32-═2 HCO3-+SO32- | B. | SO2+H2O+CO32-═H2CO3+SO32- | ||
| C. | 2SO2+2H2O+CO32-═H2CO3+2 HSO3- | D. | SO2+H2O+CO32-═HCO3-+HSO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
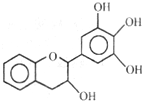 “茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂.其中没食子儿茶素( EGC )的结构如图所示.关于 EGC 的下列叙述中不正确的是( )
“茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂.其中没食子儿茶素( EGC )的结构如图所示.关于 EGC 的下列叙述中不正确的是( )| A. | 能发生加成反应、氧化反应和取代反应 | |
| B. | 遇 FeC13溶液能发生显色反应 | |
| C. | 分子中所有的原子可能共平面 | |
| D. | lmolEGC与4mo1NaOH恰好完全反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol白磷分子晶体中,含有的共价键为6mol | |
| B. | 离子晶体在熔化时,离于键被破坏,而分子晶体熔化时,化学键未被破坏 | |
| C. | 在NaCl晶体中每个Na+(或C1-)周围都紧邻6个Cl- (或Na+) | |
| D. | 由于氢键作用,HF是一种非常稳定的化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
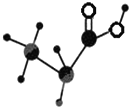 如图是某种有机物的简易球棍模型,该有机物中只含有C、H、O三种元素,下列关于该有机物的说法中正确的是( )
如图是某种有机物的简易球棍模型,该有机物中只含有C、H、O三种元素,下列关于该有机物的说法中正确的是( )| A. | 结构简式是C3H6O2 | B. | 不能和NaOH溶液反应 | ||
| C. | 官能团是羟基 | D. | 能发生取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ①④ | C. | ①③ | D. | ②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用分液的方法分离煤油和汽油 | |
| B. | 加稀盐酸后过滤,除去混在铜粉中的少量镁粉 | |
| C. | 用溶解、过滤的方法分离K2MnO4和KMnO4固体的混合物 | |
| D. | 将氧气和氢气的混合气体通过灼热的氧化铜,以除去其中的氢气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com