
| A. | 淀粉、油脂、蛋白质在一定条件下都可以发生水解反应 | |
| B. | 溴苯分子中苯环上的一个氢原子被-C4H9原子团取代形成的同分异构体共有12种 | |
| C. | 乙醇、乙酸、乙酸乙酯都能发生取代反应 | |
| D. | 乙烯、甲烷都不能使溴的四氯化碳溶液和酸性KmnO4溶液褪色 |
分析 A.淀粉水解生成葡萄糖,油脂水解生成高级脂肪酸和甘油,蛋白质水解生成氨基酸;
B.-C4H9有四种,Br与-C4H9存在邻、间、对三种位置;
C.乙酸与乙醇的酯化反应、乙酸乙酯的水解均为取代反应;
D.甲烷与溴、高锰酸钾均不反应.
解答 解:A.淀粉水解生成葡萄糖,油脂水解生成高级脂肪酸和甘油,蛋白质水解生成氨基酸,则淀粉、油脂、蛋白质在一定条件下都可以发生水解反应,故A正确;
B.-C4H9有四种,Br与-C4H9存在邻、间、对三种位置,则存在4×3=12种同分异构体,故B正确;
C.乙酸与乙醇的酯化反应、乙酸乙酯的水解均为取代反应,则乙醇、乙酸、乙酸乙酯都能发生取代反应,故C正确;
D.甲烷与溴、高锰酸钾均不反应,不能褪色,而乙烯含碳碳双键,与溴水发生加成反应,与高锰酸钾发生氧化反应,故D错误;
故选D.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系、有机反应、同分异构体的判断等为解答的关键,侧重分析与应用能力的考查,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
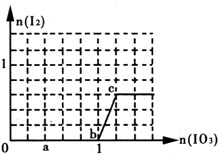
| A. | a点时消耗NaHSO3的物质的量为1.2 mol,得到的氧化产物为SO42- | |
| B. | b~c段的反应可用如下离子方程式表示:IO3-+5 I-+6H+═3I2+3H2O | |
| C. | 滴加过程中水的电离平衡一直逆向移动 | |
| D. | 从c点后所得混合液中分离出碘的操作为:加四氯化碳萃取分液,然后蒸馏 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | F2在暗处遇H2即爆炸,I2在暗处遇H2几乎不反应 | |
| B. | H2O在4000℃以上开始明显分解,H2S用酒精灯加热即可完全分解 | |
| C. | 氯与钠形成离子键,氯与硅形成共价键 | |
| D. | “NO2球”在冷水中颜色变浅,在热水中颜色加深 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X分别和其他四种元素均可形成至少2种化合物 | |
| B. | M、W、X、Y、Z的原子半径由大到小的顺序为Y>Z>X>W>M | |
| C. | X气态氢化物的稳定性大于Z态氢化物,但是X气态氢化物的沸点小于Z气态氢化物 | |
| D. | M、X、Y组成化合物和Y、Z组成化合物,它们所含的化学键类型完全相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
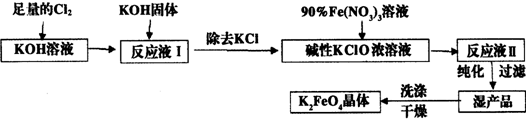
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 常温下,C(s)+H2O(g)?CO(g)+H2(g) 不能自发进行,则该反应的△H>0 | |
| B. | 25℃时,向0.1 mol•L-1CH3COOH溶液中加水稀释,$\frac{c(C{H}_{3}COOH)}{c(C{H}_{3}CO{O}^{-})}$逐渐增大 | |
| C. | Ba的金属活动性强于Mg,可以通过电解BaCl2溶液的方法获得金属钡 | |
| D. | 对硫酸工业中的反应:2SO2(g)+O2(g)?2SO3(g)△H<0,采用500℃左右的高温主要是为了加快反应速率 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com