
某反应体系的物质有:NaOH、Au2O3、Na2S4O6、Na2S2O3、Au2O、H2O.当有1mol H2O参与反应时,转移电子的物质的量为( )
|
| A. | 0.5 mol | B. | 1 mol | C. | 2 mol | D. | 4 mol |
| 氧化还原反应.. | |
| 分析: | Au2O3为反应物,则反应为Au2O3→Au2O,Au的化合价由+3价变为+1价,化合价总共降低2×2=4价,Na2S4O6中硫元素平均化合价为+2.5,Na2S2O3中硫元素平均化合价为+2,所以Na2S2O3为反应物,Na2S4O6为生成物,由于2Na2S2O3→1Na2S4O6,根据钠元素守恒可知NaOH是生成物,由氢元素守恒可知水是反应物,Na2S2O3→Na2S4O6中,S硫元素平均化合价由+2价升高为+2.5价,化合价总共升高4×(2.5﹣2)=2,根据化合价升降相等,可知Au2O3系数为1,Na2S4O6系数为2,根据元素守恒配平其它物质的系数,再根据方程式分析. |
| 解答: | 解:Au2O3为反应物,则反应中Au2O3→Au2O,Au的化合价由+3价变为+1价,化合价总共降低2×2=4价,Na2S4O6中硫元素平均化合价为+2.5,Na2S2O3中硫元素平均化合价为+2,所以Na2S2O3为反应物,Na2S4O6为生成物,由于2Na2S2O3→1Na2S4O6,根据钠元素守恒可知NaOH是生成物,由氢元素守恒可知水是反应物,Na2S2O3→Na2S4O6中,S硫元素平均化合价由+2价升高为+2.5价,化合价总共升高4×(2.5﹣2)=2,根据化合价升降相等,可知Au2O3系数为1,Na2S4O6系数为2,根据Au守恒可知Au2O系数为1,根据硫元素守恒可知Na2S2O3系数为4,根据元素Na元素守恒可知NaOH的系数为4,根据H元素守恒可知H2O系数为2, 反应方程式为Au2O3+4Na2S2O3+2H2O=Au2O+2Na2S4O6+4NaOH,则当有1mol H2O参与反应时,转移电子为2mol; 故选C. |
| 点评: | 本题考查氧化还原反应的计算、配平、基本概念等,难度中等,根据化合价、元素守恒判断反应物、生成物是解题的关键,掌握化合价升降法配平氧化还原反应方程式. |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
某研究性学习小组为研究光化学烟雾消长规律,在一烟雾实验箱中,测得烟雾的主要成分为RH(烃)、NO、NO2、O3、PAN(CH3COOONO2)及各种物质的相对浓度随时间的变化,记录于图中。根据图中数据,下列推论最不合理的是( )
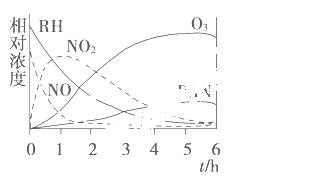
A.NO消失的速率比RH快
B.NO生成NO2
C.RH及NO2反应生成PAN及O3
D.O3生成PAN
查看答案和解析>>
科目:高中化学 来源: 题型:
已知Co2O3在酸性溶液中易被还原成Co2+,且Co2O3、Cl2、FeCl3、I2的氧化性依次减弱。下列叙述中,正确的是:
A.Cl2通入FeI2溶液中,可存在反应3Cl2+6FeI2=2FeCl3+4FeI3
B.每1 mol Co2O3在酸性溶液中被氧化生成Co2+时转移2 mol e-
mol Co2O3在酸性溶液中被氧化生成Co2+时转移2 mol e-
C.FeCl3溶液能使淀粉- KI试纸变蓝
D.I2具有较强的氧 化性,可以将Co2+氧化成Co2O3
化性,可以将Co2+氧化成Co2O3
查看答案和解析>>
科目:高中化学 来源: 题型:
分别含有下列4种杂质的纯碱样品,当含杂质的质量分数相同时,取等质量的四种样品,与浓度相同的盐酸反应,所消耗盐酸的体积由多到少的顺序是( )
杂质:①NaOH;②Ca(OH)2;③NaHCO3;④CaCO3.
|
| A. | ①②④③ | B. | ③④①② | C. | ②①④③ | D. | ④③②① |
查看答案和解析>>
科目:高中化学 来源: 题型:
某FeSO4、Fe2(SO4)3、H2SO4的混合溶液100mL,已知溶液中阳离子的浓度相同(不考虑水解),且SO42﹣的物质的量浓度为6mol/L,则此溶液最多可溶解铁粉的质量为( )
|
| A. | 11.2 g | B. | 16.8 g | C. | 19.6 g | D. | 22.4 g |
查看答案和解析>>
科目:高中化学 来源: 题型:
某校化学研究性学习小组查阅资料了解到以下内容:乙二酸(HOOC﹣COOH,可简写为H2C2O4)俗称草酸,易溶于水,属于二元中强酸,且酸性强于碳酸,其熔点为101.5℃,在157℃升华.为探究草酸的部分化学性质,进行了如下实验:
(1)向盛有1mL饱和NaHCO3溶液的试管中加入足量乙二酸溶液,观察到有无色气泡产生.该反应的离子方程式为.
(2)向盛有乙二酸饱和溶液的试管中滴入几滴硫酸酸化的KMnO4溶液,振荡,发现其溶液的紫红色褪去,说明乙二酸具有 ,请写出该反应的离子方程式:
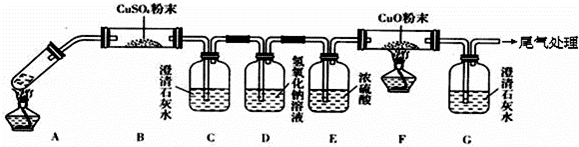
(3)将一定量的乙二酸放于试管中,按如图所示装置进行实验(夹持装置未标出):
实验发现:装置C、G中澄清石灰水变浑浊,B中CuSO4粉末变蓝,F中CuO粉末变红.据此回答:上述装置中,D的作用是 .乙二酸分解的化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
|
| A. | 含1 mol溶质的任何溶液,物质的量浓度一定相等 |
|
| B. | 配制1 mol/L NaCl溶液1 L,其方法是:将58.5 g NaCl溶于1 L水中即可 |
|
| C. | 体积相同、物质的量浓度相同的同种溶液所含溶质的粒子数一定相同 |
|
| D. | 1 L 0.5 mol/L CaCl2溶液中,Ca2+与Cl﹣的物质的量浓度都是0.5 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
对于易燃、易爆、有毒的化学物质,往往会在其包装上面贴上危险警告标签。下面所列物质,贴错了包装标签的是: ( )
| 选项 | A | B | C | D |
| 物质 | 浓硫酸 | 汽油 | 酒精 | 氯酸钾 |
| 标签 |
|
|
|
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com