
��Ԫ�����������������й㷺��Ӧ�á�
��1��Pԭ�Ӽ۵����Ų�ͼΪ__________________________��
��2����(�������)�ٷ��ӽṹ����ͼ��Pԭ���������������̬Χ������ԭ�������ϣ���ԭ�ӵ��ӻ��������Ϊ______���жϸ�������ˮ���ܽ�Ȳ����Խ���_________________________________________�������ʿ�������ͼ��ʾ����A�ĺϳɣ�����A��̼ԭ���ӻ��������Ϊ________________��һ��A����������̼ԭ����ĿΪ_______________��
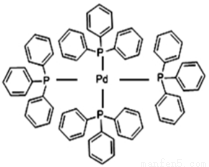
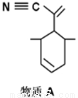
��3����ͼʾ�б�ʾ����(�������)�ٷ�������λ��
��4��PCl5��һ�ְ�ɫ���壬�ں����ܱ������м��ȿ���148 ��Һ�����γ�һ���ܵ�������壬������к���һ�����������������Ӻ�һ�����������������ӣ�������P��Cl�ļ���ֻ��198 nm��206 nm���֣����������ӵĻ�ѧʽΪ �������������������м���С��PCl3�ļ���ԭ��Ϊ____________________________���þ���ľ�������ͼ��ʾ��������ľ����߳�Ϊa pm��NAΪ����٤��������ֵ����þ�����ܶ�Ϊ_________g/cm3��
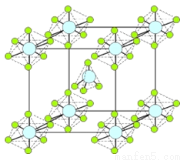
��5��PBr5��̬���ӵĽṹ��PCl5���ƣ���������Ҳ�ܵ��磬���ⶨ֪����ֻ����һ��P��Br���������õ��뷽��ʽ����PBr5�����ܵ����ԭ�� ��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꼪��ʡ�߶���ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�Լ۵��ӹ���Ϊ2s22p5��Ԫ��������ȷ���ǣ� ��
A��ԭ�Ӱ뾶��С B��ԭ������Ϊ7 C����һ��������� D���縺�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016���ຣʡ�����¸߿����һ���ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
��NA���������ӵ�������ֵ������������ȷ����
A����״���£�18g H218O����������Ϊ10NA
B��1mol�ġ�OH��1mol��OH��������������Ϊ10NA
C�����³�ѹ�£�42g��ϩ�Ͷ�ϩ��������У����Լ���Ϊ6NA
D��Na2O2��H2O�ķ�Ӧ�У�ÿ����0.1mol O2ת�Ƶ�����ĿΪ0.4NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016����������һ�и�����ģ���ۻ�ѧ�Ծ��������棩 ���ͣ������
ˮ��һ����Ҫ����Ȼ��Դ���������������治��ȱ�ٵ����ʡ���ش��������⣺
��1��ˮ������ֱ��Ӱ�����彡������Ȼˮ�ھ������������м���Ļ�����������_______________(���������ʵ�����)���侻ˮ���õ�ԭ����_______________________��
��2��ˮ�ľ�����������������______________________________________��
��3��Ӳ��Ϊ1���ˮ��ָÿ��ˮ��10 mg CaO����֮�൱������(��7.1 mg MgO)����ij��Ȼˮ��c(Ca2+)=1.2��10-3mol��L-1��c(Mg2+)=6��10-4mol��L-1�����ˮ��Ӳ��Ϊ________��
��4������3���е���Ȼˮ������c(HCO3-)=8��10-4mol��L-1����Ҫ����10 m3������Ȼˮ�������ȼ���Ca(OH)2_______g�������Na2CO3_______g��
��5����ͼ�ǵ�������������ˮ��ԭ��ͼ�����е缫A��ֱ����Դ���������缫B��ֱ����Դ�ĸ�����

�ٸ�ĤA��________(�����������)���ӽ���Ĥ��
��ij�ֺ�ˮ��Ʒ�����������д�����Na+��Cl-�Լ�������K+��SO42-����������װ�öԸú�ˮ���е�����������������ɺ�A��B��C������������Һ(��Һ��)��pH�ֱ�ΪpHa��pHb��pHc�������С˳��Ϊ__________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016����������һ�и�����ģ���ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����й�˵������ȷ����
A��ij�¶�ʱ�Ļ����Һ��c(H+)= mol��L-1��˵������Һ������(KwΪ���¶�ʱˮ�����ӻ�����)
mol��L-1��˵������Һ������(KwΪ���¶�ʱˮ�����ӻ�����)
B����ˮ�������c(H+)=10-12mol��L-1����Һ��:Na+��Ba2+��HCO3-��Cl-���Դ�������
C����֪Ksp(AgCl)=1.56��10-10�� Ksp(Ag2CrO4)=9.0��10-12������Cl-��CrO42-��Ũ�Ⱦ�Ϊ0.010 mol��L-1��Һ����μ���0.010 mol��L-1��AgNO3��Һʱ��CrO42-�Ȳ�������
D��������pH=7��CH3COOH��NaOH�����Һ�У�c(Na+)>c(CH3COO-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016������ʡ������ģ���ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵������ȷ����( )
A����֬����������Ӧ�����ɸ���
B����Ȳ����ϩ��(CH2=CHCOOH)��������ϩ��(CH3COOCH=CH2)������Ϊ�ϳɾۺ���ĵ���
C�����Ǽ���ˮ��������������������ͭ��Ӧ���ɺ�ɫ����
D���Ȱ������  ��������γ�2�ֶ���(�����������칹)
��������γ�2�ֶ���(�����������칹)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�콭��ʡ����ȫ��ģ�����ۻ�ѧ�Ծ��������棩 ���ͣ������
�л���F�ĺϳ�·����ͼ��ʾ��
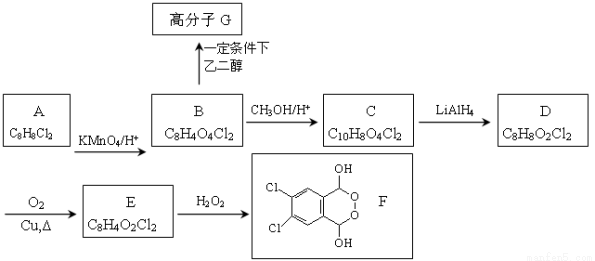
��֪������Ϣ��
��1��RCOOR�� RCH2OH
RCH2OH
��2��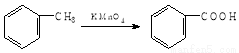
�ش��������⣺
��1��A�Ľṹ��ʽΪ ��G�Ľṹ��ʽΪ ��
��2��B����C�Ļ�ѧ����ʽΪ ��
��3������E�к��������ŵ��Լ��� ��
��Ӧ������ ��
��4��E��F�ķ�Ӧ������ ��
��5��A��ͬ���칹���У���������������ͬ���칹���� ��(������A)��д������һ�ֵĽṹ��ʽ ��
�����ڷ����廯����
�ڱ��������ĸ�ȡ����
�۱����ϵ�һ��ȡ����ֻ��һ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡɳ�С�ɳ�����и߿�ģ�����ۻ�ѧ�Ծ��������棩 ���ͣ������
�ۺ�����CO2��CO�Թ�����̼�������Ҫ���塣
��1�� Li4SiO4�����ڸ����õ���Ũ��CO2��ԭ���ǣ���500�棬��Ũ��CO2��Li4SiO4�Ӵ�������������Σ�ƽ��������700�棬��Ӧ������У��ų���Ũ��CO2��Li4SiO4������700��ʱ��Ӧ�Ļ�ѧ����ʽΪ_________________________________��
��2�� �������������(SOEC)���ڸ��µ��CO2��H2O���ȿɸ�Ч�Ʊ��ϳ���(CO��H2)���ֿ�ʵ��CO2�ļ��ţ��乤��ԭ������ͼ��

�� bΪ��Դ��________(�������������)��
�� д���缫c�����ĵ缫��Ӧʽ�� __________ ______�� __________________ ______��
��3��������ɵĺϳ����ڴ��������·������·�Ӧ��CO(g)��2H2(g)  CH3OH(g)���Դ˷�Ӧ���������о���
CH3OH(g)���Դ˷�Ӧ���������о���
ij�¶�����һ��ѹ�����зֱ����1.2 mol CO��1 mol H2���ﵽƽ��ʱ�������Ϊ2 L���Һ���0.4 mol CH3OH(g)����÷�Ӧƽ�ⳣ��ֵΪ________����ʱ����������ͨ��0.35 mol CO���壬���ƽ�⽫________(�������Ӧ�������������淴Ӧ����)�ƶ���
��4�� ��֪��

���״���ȼ����Ϊ��H3�����æ�H1����H2����H3��ʾCO(g)��2H2(g)  CH3OH(l)�Ħ�H��
CH3OH(l)�Ħ�H��
��H��______ ____��
��5������̫���ܺ�ȱ��������[��Fe0.9O]�ɽ�����CO2�Ƚ�Ϊ̼��������ʵ��CO2����Դ����ת�� ��������ͼ��ʾ������1 molȱ��������[Fe0.9O]������CO2��ȫ��Ӧ������________mol C(̼)��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�����ʡ��һ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
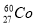 ��r���ߵķ���Դ������
��r���ߵķ���Դ������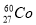 ��˵����ȷ���ǣ� ��
��˵����ȷ���ǣ� ��
A��������Ϊ 33 B��������Ϊ27 C��������Ϊ60 D���˵����Ϊ60
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com