
有下列四种微粒:①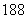 O ②
O ②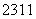 Na ③
Na ③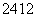 Mg ④
Mg ④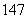 N(用序号填空)。
N(用序号填空)。
(1)按原子半径由大到小顺序排列是________________________________________________________________________。
(2)微粒中质子数小于中子数的是________________________________________________________________________。
(3)在化合物中呈现的化合价的数值最多的是________________________________________________________________________。
(4)能形成X2Y2型化合物的是________,能形成X3Y2型的化合物的是________。
解析:(1)由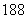 O、
O、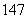 N具有2个电子层,而
N具有2个电子层,而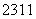 Na、
Na、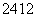 Mg具有3个电子层,因此Na、Mg的原子半径大于O、N,而对于11Na、12Mg来说,由于Mg的核电荷数大,因此r(Na)>r(Mg),同样r(N)>r(O),故原子半径由大到小排列为r(Na)>r(Mg)>r(N)>r(O)。
Mg具有3个电子层,因此Na、Mg的原子半径大于O、N,而对于11Na、12Mg来说,由于Mg的核电荷数大,因此r(Na)>r(Mg),同样r(N)>r(O),故原子半径由大到小排列为r(Na)>r(Mg)>r(N)>r(O)。
(2)由N=A-Z得中子数分别为N(O)=10、N(Na)=12、N(Mg)=12、N(N)=7。
(4)能形成X2Y2型化合物,则X可呈+1价而Y呈-1价,故为Na2O2,能形成X3Y2型化合物,则X呈+2价,Y呈-3价,故为Mg3N2。
答案:(1)②>③>④>① (2)①② (3)④
(4)①② ③④


科目:高中化学 来源: 题型:
化学在人类社会发展中起着重要的作用,展望未来,化学科学具有十分广阔的探索空间。请你分析下列四个选项中现代化学不涉及的研究领域是( )
A.开发新的能源 B.合成新的物质
C.空间形式和数量关系 D.防治环境污染
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C是三种常见的化合物,A为淡黄色固体。它们之间的转化关系如图所示:完成下列空白:
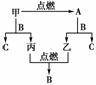
(1)A的化学式:__________,B的化学式:____________。
(2)写出甲+B―→C+丙的化学方程式:________________________________ ____________________________________________________________________________。
(3)写出A的一种重要用途:___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组元素性质的递变情况错误的是( )
A.Li、Be、B原子最外层电子数依次增多
B.P、S、Cl元素最高正价依次升高
C.N、O、F原子半径依次增大
D.Na、K的电子层数逐渐增多
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于胶体的说法中,正确的是( )
A.胶体与溶液有明显不同的外观特征,胶体呈胶状
B.胶体不稳定,静置后容易产生沉淀
C.可通过丁达尔现象鉴别胶体和溶液
D.要形成胶体,必须是符合一定结构的分散质,如氯化钠就不能形成胶体和浊液
查看答案和解析>>
科目:高中化学 来源: 题型:
关于Na2CO3和NaHCO3性质的说法,正确的是( )
A.热稳定性:NaHCO3 > Na2CO3
B.与澄清石灰水反应:Na2CO3、NaHCO3溶液中均有沉淀生成
C.相同温度时,在水中的溶解性:NaHCO3 > Na2CO3
D.等质量的NaHCO3和Na2CO3分别与足量盐酸反应,在同温同压下,生成的CO2体积相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com