
����Ŀ������ȼ�ϵ���ǵĽ�ɫ��ѧ�������ͷ���װ��,��ͼΪ���ʾ��ͼ,�õ�ص缫�����һ��ϸϸ�IJ���,�������������ǿ�������ȶ�����ش�
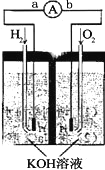
��1������ȼ�ϵ�����ת����ʽ��____,�ڵ����е��˵���������Ϊ______����a��b��ʾ��
��2��������ӦʽΪ___________
��3���õ�ع���ʱ,H2��O2�������ⲿ����,��ؿ����������ṩ����,��˴�����ȫ�����ǹؼ�����֮һ,�������һ����Ҫ�Ĵ������,����ͷ���ԭ�����£�
I .2Li+H2=2LiH; II. LiH+H2O=LiOH+H2��
�ٷ�ӦI�еĻ�ԭ����______,��ӦII�е���������______
����LiH��H2O����,�ų�224L����״����H2�������ȼ��,������ת����Ϊ80%,������ͨ�����ӵ����ʵ���Ϊ____mol;�������ĵ���������ⱥ��ʳ��ˮ,�����������������״����Ϊ_____L
���𰸡���-�� ��a��b 2H2+4OH--4e-=4H2O Li H2O 16 179.2L
��������
��1������ԭ��صĶ�����������ݵ�ʧ�����жϣ�
��2�����ݵ�ʧ����д���缫��Ӧʽ��
��3��������������Ի�ѧ��Ӧ���ʵ�Ӱ�����ط�����
��4���ٸ��ݻ��ϼ۵ı仯�жϣ�
�ڸ���ʵ�ʲμӷ�Ӧ�������Լ��缫��Ӧʽ���㣮
��1����װ�ðѻ�ѧ��ת��Ϊ���ܣ�������ԭ��أ�������Ӧʱ������ʧ���ӣ������ĵ��ӣ����Ե��ӵ���������������a��b��
�ʴ�Ϊ���ɻ�ѧ��ת��Ϊ���ܣ���a��b��
��2������������ʧ���Ӻ���������������ˮ�����Ե缫��ӦʽΪ2H2+4OH--4e-=4H2O��
�ʴ�Ϊ��2H2+4OH--4e-=4H2O��
��3����2Li+H2=2LiH�÷�Ӧ���ʧ���ӷ���������Ӧ��������ǻ�ԭ����LiH+H2O=LiOH+H2�����÷�Ӧ��H2O�õ�������������������ԭ��Ӧ������H2O����������
�ʴ�Ϊ��Li�� H2O��
����LiH��H2O���ã��ų���224L����״����H2�������ȼ�ϣ���H2���ʵ���Ϊ10mol����ʵ�ʲμӷ�Ӧ��H2Ϊ10mol��80%=8mol��1molH2ת����1molH2O��ת��2mol���ӣ�����8molH2��ת��16mol�ĵ��ӣ������ĵ���������ⱥ��ʳ��ˮ���������������ʵ�����8mol���������������V=n��Vm=8mol��22.4L/mol=179.2L��
�ʴ�Ϊ��16��179.2L��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�˵����ȷ����
A. ��֪HI(g) ![]() 1/2H2(g)��1/2I2(s)����H����26.5 kJ��mol��1���ɴ˿�֪1 mol HI�������ܱ������г�ַֽ����Էų�26.5 kJ������
1/2H2(g)��1/2I2(s)����H����26.5 kJ��mol��1���ɴ˿�֪1 mol HI�������ܱ������г�ַֽ����Էų�26.5 kJ������
B. ��֪2H2(g)��O2(g)===2H2O(g)����H����571.6 kJ��mol��1����������ȼ����Ϊ��H����285.8 kJ��mol��1
C. ��֪2C(s)��2O2(g)=2CO2(g) ��H1, 2C(s)��O2(g)=2CO(g) ��H2������H1����H2
D. ��20.0 g NaOH��ϡ��Һ��ϡ������ȫ�кͣ��ų�28.7 kJ����������ϡ�����ϡNaOH��Һ��Ӧ���Ȼ�ѧ����ʽΪ��NaOH(aq)��CH3COOH(aq)===CH3COONa(aq)��H2O(l)����H����57.4 kJ��mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��ڱ���������ȷ���ǣ� ��
A.���ķ���ʽΪC6H6��������ʹ����KMnO4��Һ��ɫ�����ڱ�����
B.�ӱ��Ŀ�����ʽ(![]() )�����������к���̼̼˫����Ӧ����ϩ��
)�����������к���̼̼˫����Ӧ����ϩ��
C.�ڴ��������£�����Һ�巴Ӧ�����屽�������˼ӳɷ�Ӧ
D.������Ϊƽ���������νṹ��6��̼ԭ��֮��ļۼ���ȫ��ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ݻ�һ�����ܱ������У�����һ������NO(g)������C(s)��������ӦC(s)��2NO(g) ![]() CO2(g)��N2(g)��ƽ��״̬ʱNO(g)�����ʵ���Ũ��[NO]���¶�T�Ĺ�ϵ��ͼ��ʾ��������˵������ȷ����(����)
CO2(g)��N2(g)��ƽ��״̬ʱNO(g)�����ʵ���Ũ��[NO]���¶�T�Ĺ�ϵ��ͼ��ʾ��������˵������ȷ����(����)
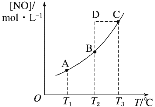
A. �÷�Ӧ����H>0
B. ���÷�Ӧ��T1��T2ʱ��ƽ�ⳣ���ֱ�ΪK1��K2����K1<K2
C. ��T2ʱ������Ӧ��ϵ����״̬D�����ʱһ����v��<v��
D. ��T3ʱ�������������ܶȲ��ٱ仯��������жϷ�Ӧ�ﵽƽ��״̬C
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶��£���pH=6������ˮ�м���NaHSO4���壬�����¶Ȳ��䣬�����Һ��pHΪ2�����ж��ڸ���Һ����������ȷ����
A. ���¶ȸ���25��
B. ��ˮ���������H+��Ũ����1.0��10-12 mol��L-1
C. ����NaHSO4����������ˮ�ĵ���
D. c(H+)=c(OH-)+ c(SO42-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������(K2FeO4)��һ�����ͷ��ȸ�Ч������������KOH��Һ�����ȶ��Բʵ�����Ʊ�������ص�ԭ��Ϊ3Cl2+2Fe(OH)3+10KOH==2K2FeO4+6KCl++8H2O������ʵ����Ʋ��ܴﵽʵ��Ŀ�ĵ���
A.��ͼ ��ʾװ���Ʊ�����������
��ʾװ���Ʊ�����������
B.��ͼ ��ʾװ���Ʊ��������
��ʾװ���Ʊ��������
C.��ͼ ��ʾװ�÷����������ش�Ʒ
��ʾװ�÷����������ش�Ʒ
D.��ͼ ��ʾװ�ø���������
��ʾװ�ø���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ݱ������ҹ���ѧ�о���Ա��Ni(NO3)2��Tb(CH3COO)3�Ⱥϳ���һ������һά��״��λ�ۺ���(��ͼ)������������ڴ��ԡ��绯ѧ���ʵȷ�����о����������ָ����

��ش��������⣺
(1)��̬Niԭ�ӵļ۵��ӹ������ʽΪ____________��Ni��Ԫ�����ڱ��д��ڵ�____________���С�
(2)C��N��O����Ԫ���е縺��������____(��Ԫ�ط���)��C���γɻ�����ʱ��������Թ��ۼ�Ϊ����ԭ����_____________��
(3)Ni(NO3)2�������ӵĿռ乹����______��д����������ӻ�Ϊ�ȵ������һ�ַ��ӵĻ�ѧʽ��________��
(4)һά��״��λ�ۺ����У�̼ԭ�ӵ��ӻ���ʽΪ________________________��
(5)��֪�� CH3COOH�ķе�Ϊ117.9���� HCOOCH3�ķе�Ϊ32����CH3COOH�ķе���� HCOOCH3����Ҫԭ����______��
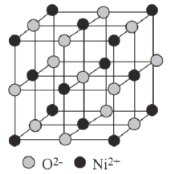
(6)��֪���������ľ����ṹ��ͼ��ʾ��
����NAΪ�����ӵ�������ֵ�������ܶ�Ϊ��g��cm��3����þ����������O2��֮��ľ���Ϊ____pm(�ú�����NA�Ĵ���ʽ��ʾ)��
��ijȱ�������������Ϊ Ni0.97O������NiԪ��ֻ��+2��+3���ּ�̬�����ּ�̬����������Ŀ֮��Ϊ___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ������� WO3 ����ϩ�� 2-��ϩ�ϳɱ�ϩ�ķ�Ӧ������ͼ������̼ԭ�����������˵��ӽṹ��������˵������ȷ����
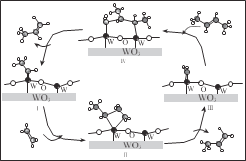
A.��ϩ����ϩ�� 2-��ϩ��Ϊͬϵ��
B.��ϩ����ϩ�� 2-��ϩ�ķе���������
C.������м���� 2-��ϩ���з�ʽ�ṹ
D.̼���٣�W��ԭ�Ӽ�Ļ�ѧ���ڢ��������Ĺ�����δ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ӦA2(g)+B2(g)=2AB(g)�������仯��ͼ��ʾ������������ȷ���ǣ� ��

A.�÷�Ӧ�Ƿ��ȷ�Ӧ
B.��ͼ��֪��1molA2(g)��1molB2(g)��Ӧ����2molAB(g)�ų�bkJ����
C.��ͼ��֪��1molA2(g)��1molB2(g)��Ӧ����2molAB(g)����bkJ����
D.��ͼ��֪��1molA2(g)��1molB2(g)��Ӧ����2molAB(g)����(a-b)kJ����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com