
【题目】下列说法正确的是( )
A.H2(g)+I2(g) 2HI(g),其他条件不变,缩小反应容器体积,正逆反应速率不变
B.C(s)+H2O(g) H2(g)+CO(g),气体的总物质的量不再改变不能说明反应已达平衡
C.若压强不再随时间变化能说明反应2A(?)+B(g) 2C(?)已达平衡,则A、C不能同时是气体
D.1 mol N2和3 mol H2反应达到平衡时H2转化率为10%,放出的热量为Q1;在相同温度和压强下,当2 mol NH3分解为N2和H2的转化率为10%时,吸收的热量为Q2,Q2等于Q1
【答案】D
【解析】
A. H2(g)+I2(g) 2HI(g),其他条件不变,缩小反应容器体积增大压强,则正逆反应速率均增大,A错误;
B. C(s)+H2O(g) H2(g)+CO(g),气体的总物质的量会随着反应而变化,当其不再改变时则能说明反应已达平衡,B错误;
C. 2A(?)+B(g) 2C(?)的两边,气体分子总数不可能相等,故不管A、C是什么状态,若压强不再随时间变化均能说明反应2A(?)+B(g) 2C(?)已达平衡,C错误;
D. 设合成氨反应中消耗1 mol N2和3 mol H2同时生成2 mol NH3时,放出热量为Q,则热化学方程式为:![]() ,消耗2 mol NH3同时生成1 mol N2和3 mol H2时,吸收热量为Q,则热化学方程式为:
,消耗2 mol NH3同时生成1 mol N2和3 mol H2时,吸收热量为Q,则热化学方程式为:![]() ,当1 mol N2和3 mol H2反应达到平衡时H2转化率为10%,放出的热量为Q1=0.1Q,在相同温度和压强下,当2 mol NH3分解为N2和H2的转化率为10%时,吸收的热量为Q2=0.1Q,D正确;
,当1 mol N2和3 mol H2反应达到平衡时H2转化率为10%,放出的热量为Q1=0.1Q,在相同温度和压强下,当2 mol NH3分解为N2和H2的转化率为10%时,吸收的热量为Q2=0.1Q,D正确;
答案选D。


 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案科目:高中化学 来源: 题型:
【题目】如图是元素周期表的一部分,请回答下列问题:
IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0族 | |
1 | ① | |||||||
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(1)在这些元素中,单质的化学性质最不活泼的是______________(填元素符号)。
(2)③的气态氢化物的电子式______________,②④形成的可溶于水的气态化合物的结构式______________。
(3)这些元素形成的最高价氧化物的水化物中,碱性最强的化合物为______________(填物质的化学式),酸性最强的含氧酸为______________(填物质的化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】既可以用来鉴别甲烷和乙烯,又可以用来除去甲烷中混有的少量乙烯的操作方法是( )
A. 混合气体通过盛有酸性高锰酸钾溶液的洗气瓶
B. 混合气体通过盛有足量溴水的洗气瓶
C. 混合气体通过盛有蒸馏水的洗气瓶
D. 混合气体与适量氯化氢混合
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验对应现象及结论有错误的是( )
选项 | 实验 | 现象 | 结论 |
A | 向AgCl悬浊液中加入KI溶液,振荡 | 沉淀由白色变为黄色 | AgCl溶解度大于AgI |
B | 向2mL0.1mol/L的FeCl3溶液中加足量铁粉,振荡,加1滴KSCN溶液 | 黄色逐渐消失,加KSCN溶液颜色不变 | 还原性:Fe>Fe2+ |
C | 常温下,向等体积、等浓度的NaHCO3和CH3COONa溶液中分别滴加2滴酚酞 | 两份溶液均变红,NaHCO3溶液红色更深 | 常温下的水解平衡常数: Kh(CH3COO-)<Kh(HCO3-) |
D | 常温时,用两支试管各取4mL 0.1mol/L 酸性KMnO4溶液,分别加入0.1mol/L和0.2 mol/L H2C2O4溶液各2 mL | 两试管溶液均褪色,且加0.2mol/L H2C2O4 溶液的试管中褪色更快 | 其它条件不变,H2C2O4溶液的浓度越大,化学反应速率越大 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】LED系列产品是被看好的一类节能新产品,下图是一种氢氧燃料电池驱动LED发光的装置。下列有关叙述正确的是
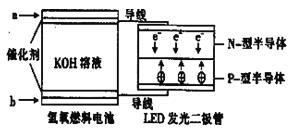
A.a处通入氢气,发生了还原反应:H2-2e-+2OH-=2H2O
B.b处通入氧气,为电池的正极
C.该装置中只涉及两种形式的能量转化,电池中的KOH溶液也可用稀硫酸溶液代替
D.P-型半导体连接的是电池负极.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)家用液化石油气的主要成分之一是甲烷,当16 kg甲烷完全燃烧并生成二氧化碳气体和液态水时,放出的热量为8.9×105 kJ。已知1mol液态水汽化时需要吸收44 kJ热量。试写出甲烷燃烧生成水蒸气的热化学方程式: 。
(2)有同学用甲烷与空气为原料制作一燃烧电池,若以稀硫酸为电解质溶液时,其负极反应式为 。
(3)已知拆开1 mol H-H键,1 molN-H键,1 molN≡N键分别需要的能量是akJ、bkJ、ckJ,则N2与H2反应生成NH3的热化学方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据以下转化关系,完成以下各空:
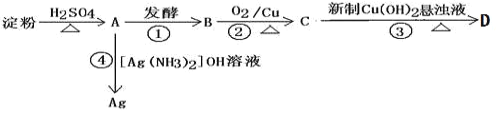
(1) A和C的结构简式:A__________________C________________。
(2) 写出②③的化学方程式:
②_______________________________________________________
③________________________________________________________
(3)④的反应类型_____________
(4)C2H518OH与D酸化后的产物反应的化学方程式______________________。
(5)用饱和碳酸钠溶液收集乙酸乙酯后,分离得到乙酸乙酯的方法是__________,分离需要的玻璃仪器有________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高血脂是一种常见的心血管疾病,治疗高血脂的新药I的合成路线如下:

已知:a、
b、
回答下列问题:
(1)反应①所需试剂、条件分别是____________;F 的化学名称为____________。
(2)②的反应类型是______________;A→B 的化学方程式为_________________。
(3)E的结构简式为______________;H 中所含官能团的名称是____________。
(4)化合物W 的相对分子质量比化合物C 大14,且满足下列条件,W 的可能结构有____种。①遇FeCl3 溶液显紫色;②能发生银镜反应,其中核磁共振氢谱显示有5 种不同化学环境的氢,峰面积比为2:2:2:1:1,写出符合要求的W 的结构简式____________。
(5)设计用甲苯和乙醛为原料制备![]() 的合成路线,其他无机试剂任选(合成路线常用的表示方式为:A
的合成路线,其他无机试剂任选(合成路线常用的表示方式为:A![]() B。。。
B。。。![]() 目标产物。____________。
目标产物。____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】类推思维是化学解题中常用的一种思维方法,下列有关离子方程式的类推正确的是)
选项 | 已知 | 类推 |
A | 将Fe加入CuSO4溶液中:Fe+Cu2+=== Cu+Fe2+ | 将Na加入到CuSO4溶液中:2Na+Cu2+=== Cu+2Na+ |
B | 向Ca(ClO)2溶液中通入少量CO2:CO2+H2O+Ca2++2ClO-=== CaCO3↓+2HClO | 向Ca(ClO)2溶液中通入少量SO2:SO2+H2O+Ca2++2ClO-=== CaSO3↓+2HClO |
C | 惰性电极电解氯化钠溶液:2Cl-+2H2O | 惰性电极电解MgBr2溶液:2Br-+2H2O |
D | 稀盐酸与NaOH溶液反应至中性:H++OH-===H2O | 稀硝酸与Ba(OH)2溶液反应至中性:H++OH-===H2O |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com