


科目:高中化学 来源: 题型:
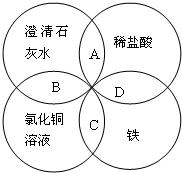 铁、稀盐酸、澄清石灰水、氯化铜溶液是中学化学中常见物质,四种物质间的反应关系如图所示.图中两圆相交部分(A、B、C、D)表示物质间的反应,其中对应反应的离子方程式书写正确的是( )
铁、稀盐酸、澄清石灰水、氯化铜溶液是中学化学中常见物质,四种物质间的反应关系如图所示.图中两圆相交部分(A、B、C、D)表示物质间的反应,其中对应反应的离子方程式书写正确的是( )| A、OH-+HCl=H2O+Cl- |
| B、Ca(OH)2+Cu2+=Ca2++Cu(OH)2↓ |
| C、Fe+Cu2+=Cu+Fe2+ |
| D、Fe+2H+=Fe3++H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、测定HCl和NaOH反应的中和热时,每次实验均应测量3个温度,即盐酸起始温度、NaOH起始温度和反应后终止温度 |
| B、在101 kPa时,1 mol H2完全燃烧生成液态水,放出285.8 kJ热量,H2的燃烧热为:-285.8kJ?mol-1 |
| C、在101 kPa时,1 mol C与适量O2反应生成1 mol CO时,放出110.5 kJ热量,则C的燃烧热为110.5 kJ?mol-1 |
| D、生成物总能量一定低于反应物总能量,同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件下的△H不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氧化物 | B、难溶于水 |
| C、属于硅酸盐 | D、属于纯净物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 在过量的盐酸中加入等质量的锌在不同的试验条件下进行反应,测定在不同时间t产生氢气体积v的数据,根据数据绘制得到图1,则曲线a、b、c、d所对应的试验( )
在过量的盐酸中加入等质量的锌在不同的试验条件下进行反应,测定在不同时间t产生氢气体积v的数据,根据数据绘制得到图1,则曲线a、b、c、d所对应的试验( ) | 组别 | c(HCl)(mol?L-1) | 温度(℃) | 状态 |
| 1 | 2.0 | 25 | 块状 |
| 2 | 2.5 | 30 | 块状 |
| 3 | 2.5 | 50 | 粉末状 |
| 4 | 2.5 | 30 | 粉末状 |
| A、4-3-1-2 |
| B、1-2-3-4 |
| C、1-2-4-3 |
| D、3-4-2-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 反应物 |
| 反应条件 |
| 反应物 |
| 反应条件 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该溶液可由等物质的量浓度、等体积的氨水溶液和盐酸溶液混合而成 |
| B、该溶液可由pH=2的HCl与pH=12的氨水等体积混合而成 |
| C、加入适量的盐酸,溶液中离子浓度为c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
| D、加入适量CH3COOH溶液,c(NH4+)一定大于c(Cl-)、c(CH3COO-)之和 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com