
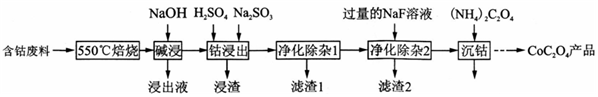
分析 550℃焙烧含钴废料(主要成分为Co2O3,含少量Fe2O3、Al2O3、CaO、MgO、碳及有机物等)除去碳和有机物,加入氢氧化钠溶液,其中Al2O3溶解生成NaAlO2,Co2O3、Fe2O3、Al2O3、CaO、MgO不溶,过滤,则浸出液的主要为NaAlO2,向过滤得到的固体加入稀硫酸和亚硫酸钠,Na2SO3将Co3+、Fe3+还原为Co2+、Fe2+,可得CoCl2、FeCl2、MgCl2、CaCl2,在40~50℃加入H2O2,氧化Fe2+氧化为Fe3+,再升温至80~85℃,加入Na2CO3调pH至4.5,可得到Fe(OH)3沉淀,过滤后所得滤液主要含有CoCl2、MgCl2、CaCl2,用NaF溶液除去钙、镁,过滤后,滤液中主要含有CoCl2,加入草酸铵溶液得到草酸钴,据此分析解答.
解答 解:(1)“550℃焙烧”可以除去碳和有机物;
故答案为:除去碳和有机物;
(2)加入氢氧化钠溶液,Al2O3溶解生成NaAlO2,所以浸出液的主要成分为NaAlO2;
故答案为:NaAlO2;
(3)“钴浸出”过程中Co3+转化为Co2+,则Na2SO3将Co3+还原为Co2+,自身被还原为硫酸钠,发生的反应为:2Co3++SO32-+H2O=2Co2++SO42-+2H+;
故答案为:2Co3++SO32-+H2O=2Co2++SO42-+2H+;
(4)加入H2O2,氧化Fe2+氧化为Fe3+,反应为:2Fe2++2H++H2O2=2Fe3++2H2O,再升温至80~85℃,加入Na2CO3调pH至4.5,可得到Fe(OH)3沉淀;
故答案为:2Fe2++2H++H2O2=2Fe3++2H2O;Fe(OH)3;
(5)已知Ksp(MgF2)=7.35×10-11、Ksp(CaF2)=1.05×10-10,若所得滤液中c(Ca2+)=1.0×l0-5mol/L,则c(F-)2=$\frac{Ksp(Ca{F}_{2})}{c(C{a}^{2+})}$,c(Mg2+)=$\frac{Ksp(Mg{F}_{2})}{c({F}^{-})^{2}}$=$\frac{Ksp(Mg{F}_{2})•c(C{a}^{2+})}{Ksp(Ca{F}_{2})}$=7.0×10-6mol/L;
故答案为:7.0×10-6mol/L;
(6)称取1.00g样品,将其用适当试剂转化,得到草酸铵[(NH4)2C2O4]溶液,再用过量稀硫酸酸化,用0.1000mol/L KMnO4溶液滴定,达到滴定终点时,共用去KMnO4溶液26.00mL,
根据5CoC2O4~5(NH4)2C2O4~2KMnO4,则样品中m(CoC2O4)=$\frac{5}{2}$×26×10-3L×0.1mol/L×147g/mol=0.9555g,故酸钴样品的纯度为$\frac{0.9555}{1.0}×100%$=95.55%;
故答案为:95.55%.
点评 本题考查物质制备工艺流程、物质的分离提纯、溶度积常数应用等,侧重考查学生分析能力、获取信息能力,难度较大.


 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案科目:高中化学 来源: 题型:选择题
| A. | 东晋葛洪《肘后备急方》中记载了“青蒿一握,以水二升渍,绞取汁,…”,此过程属于物理变化 | |
| B. | 日本福岛核电站事故中,核原料裂变产生的2种放射性同位素碘-131和铯-137的中子数不同 | |
| C. | 乙烯与氧气在银催化作用下生成环氧乙烷符合绿色化学的原子经济性要求 | |
| D. | PM2.5是指天气中直径接近2.5×10-6m的颗粒物,其分散在空气中形成胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验方案 | 现象 | 结论 |
| A | 向SiO2固体中加入足量盐酸 | 固体不溶解 | SiO2不溶于任何酸 |
| B | 向Na2CO3溶液中通入足量CO2 | 产生晶体 | 溶解度:NaHCO3>Na2CO3 |
| C | 向75%的酒精中加入小粒钠 | 产生气泡 | 乙醇与钠反应产生H2 |
| D | 向KI 淀粉溶液中通入气体X | 溶液变蓝 | X的氧化性比I2的氧化性强 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | M的分子式为C9H10O4 | |
| B. | M与浓溴水既能发生取代反应,又能发生加成反应 | |
| C. | 一定条件下,1 mol M最多能与3molH2发生反应 | |
| D. | M能分别与Na、NaOH、NaHCO3发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | A | B | C | D |
| 关系 | 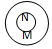 包含关系 | 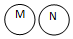 并列关系 | 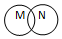 交集关系 |  重叠关系 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | FeCl2有氧化性,能用于雕刻电路板 | |
| B. | 金刚石是自然界中硬度最大的物质,不与氧气发生反应 | |
| C. | 明矾加入水中能形成Al(OH)3胶体,可用作净水剂 | |
| D. | SiO2不与强酸反应,可用石英器皿盛装氢氟酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径 A>B>D>C | B. | 原子序数 d>c>b>a | ||
| C. | 离子半径 C>D>B>A | D. | 阴离子的还原性C2-<D- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH2=CHCOOH、CH3COOCH=CH2均可作为合成聚合物的单体 | |
| B. | C6Hn分子中的六个碳原子在同一直线上,则n可能等于2 | |
| C. | 2,2-二甲基丁烷与2,4-二甲基戊烷的一氯代物种类相同 | |
| D. | 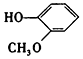 与 与 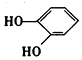 都是酚且互为同系物 都是酚且互为同系物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com