
(5分)对无机化合物可根据其组成和性质进行如下分类:
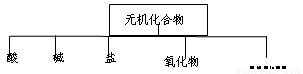
(1)上图所示的物质分类方法可称为 。
(2)以Na、H、C、N、O、S、Cl等元素中任选两种或三种元素组成合适的一种物质,将其化学式分别填在下表中的相应位置。
物质 类别 | 酸 | 碱 | 盐 | 氧化物 |
化学式 |
|
|
|
|
 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案科目:高中化学 来源: 题型:
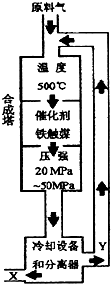 合成氨反应(N2+3H2?2NH3+92.4KJ)在化学工业和国防工业具有重要意义.工业合成氨生产示意图如图所示.
合成氨反应(N2+3H2?2NH3+92.4KJ)在化学工业和国防工业具有重要意义.工业合成氨生产示意图如图所示.查看答案和解析>>
科目:高中化学 来源:2013年普通高等学校招生全国统一考试化学(广东卷解析版) 题型:选择题
下列叙述I和II均正确并且有因果关系的是
选项 | 陈述I | 陈述II |
A | NH4Cl为强酸弱碱盐 | 用加热法除去NaCl中的NH4Cl |
B | Fe3+具有氧化性 | 用KSCN溶液可以鉴别Fe3+ |
C | 溶解度:CaCO3<Ca(HCO3)2 | 溶解度:Na2CO3<NaHCO3 |
D | SiO2可与HF反应 | 氢氟酸不能保存在玻璃瓶中 |
查看答案和解析>>
科目:高中化学 来源:2013-2014北京市房山区下学期高二期末测验化学试卷(解析版) 题型:选择题
下列溶液,按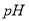 由小到大顺序排列的是
由小到大顺序排列的是
① 溶液②
溶液②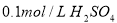 溶液
溶液
③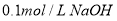 溶液④
溶液④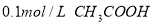 溶液
溶液
A. ①②④③B. ②①④③C. ③④①②D. ④③②①
查看答案和解析>>
科目:高中化学 来源:2014秋季江西省赣州市十二县高一上学期期中联考化学试卷(解析版) 题型:选择题
已知硫酸的质量分数越大时,其溶液的密度越大;已知98%的浓硫酸的浓度为18.4mol/L,则49%的硫酸溶液的浓度为
A.9.2 mol/L B.>9.2 mol/L
C.<9. 2 mol/L D.无法确定
查看答案和解析>>
科目:高中化学 来源:2014秋北京市高一上学期期中化学试卷(解析版) 题型:填空题
(8分)实验室要配制200mL 1mol/L NaOH溶液,请回答下列问题。
(1)用托盘天平称取氢氧化钠,其质量为 克。
(2)实验开始前,需要检查容量瓶是否 。
(3)下列主要操作步骤的正确顺序是 。
①称取一定量的氢氧化钠,放入烧杯中,用适量的蒸馏水溶解;
②用胶头滴管向容量瓶中加入蒸馏水至凹液面与刻度线相切;
③待冷却至室温后,将溶液转移到容量瓶中;
④盖好瓶塞,反复上下颠倒,摇匀;
⑤用少量的蒸馏水洗涤烧杯内壁和玻璃棒2至3次,洗涤液转移到容量瓶中。
(4)在配制过程中,其他操作都正确,下列操作会引起所配溶液浓度偏低的是: (填序号)
①溶解NaOH固体的过程中,有少量溶液溅出烧杯
②容量瓶不干燥,含有少量蒸馏水
③用于溶解NaOH的烧杯、玻璃棒未洗涤
④定容摇匀后发现液体体积小于刻度线,未补加少量蒸馏水至刻度线
(5)下图是该同学转移溶液的示意图,
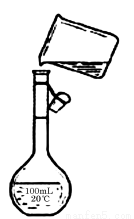
图中的错误是 , 。
查看答案和解析>>
科目:高中化学 来源:2014秋北京市高一上学期期中化学试卷(解析版) 题型:选择题
用NA表示阿伏德罗常数,下列叙述正确的是
A.常温常压下,1.06g Na2CO3含有的Na+离子数为0.02NA
B.标准状况下,22.4LH2O含有的分子数为NA
C.通常状况下,NA 个CO2分子占有的体积为22.4L
D.物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl- 个数为NA
查看答案和解析>>
科目:高中化学 来源:2014~2015学年重庆市9月月考高一化学试卷(解析版) 题型:实验题
(14分)某实验小组用0.50 mol·L- 1 NaOH溶液和0.50mol·L- 1 的硫酸溶液进行中和热的测定。
 Ⅰ.配制0.50mol·L- 1 硫酸溶液
Ⅰ.配制0.50mol·L- 1 硫酸溶液
(1)若配制250 mL硫酸溶液,则须用量筒量取密度为1.84 g·cm- 3、质量分数为98%的浓硫酸 mL。
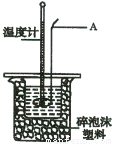
Ⅱ.测定稀硫酸和稀氢氧化钠溶液中和热的实验装置如右图所示:
(2)仪器A的名称为 ;
(3)装置中碎泡沫塑料的作用是 ;
(4)写出该反应中和热的热化学方程式:(中和热为57.3 kJ·mol- 1) ;
(5)取50 mL NaOH溶液和30 mL硫酸溶液进行实验,实验数据如下表。
①下表中的温度差平均值为 ℃;
②近似认为0.50mol·L- 1 NaOH溶液和0.50mol·L- 1 硫酸溶液的密度都是1g·cm- 3 ,中和后生成溶液的比热容c= 4.18 J·(g·℃)- 1 。则中和热△H= (取小数点后一位)。
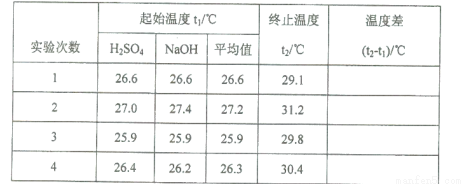
③上述实验数值结果与57.3 kJ·mol- 1 有偏差,产生此实验偏差的原因可能是(填字母) 。
A.实验装置保温、隔热效果差
B.量取NaOH溶液的体积时仰视读数
C.一次性把NaOH溶液倒入盛有硫酸的小烧杯中
D.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com