
| 10-a |
| 10-11 |
| 10-a |
| 10-11 |
| 0.04mol-0.02mol |
| 0.2L |
| 10-13 |
| 0.1 |


科目:高中化学 来源: 题型:
| A、H+、Na+、NO3-、Fe2+ |
| B、Na+、K+、NH4+、H+ |
| C、K+、NH4+、NO3-、OH- |
| D、H+、K+、NO3-、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
 ③CH3CH2Br ④
③CH3CH2Br ④ ⑤
⑤ ⑥
⑥ ⑦
⑦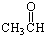 ⑧
⑧ ⑨
⑨ ⑩
⑩
查看答案和解析>>
科目:高中化学 来源: 题型:
 将Na2CO3和NaHCO3的混合物共19克,加热到质量不再发生变化时,称得剩余固体质量为15.9克.则
将Na2CO3和NaHCO3的混合物共19克,加热到质量不再发生变化时,称得剩余固体质量为15.9克.则查看答案和解析>>
科目:高中化学 来源: 题型:

| 化学键 | H-H | N≡N |
| 键能/kJ?mol-1 | 435 | 943 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、其单质与水反应的通式为:X2+H2O→HX+HXO |
| B、HX易溶于水,其水溶液是强酸 |
| C、HX都可用相应的NaX与浓硫酸共热制取 |
| D、按F、Cl、Br、I的顺序,其单质的氧化性逐渐减弱,阴离子的还原性逐渐增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、还原性:F-<Cl-<Br-<I- |
| B、微粒半径:F->Na+>Mg2+>Al3+ |
| C、酸性HClO4>HClO3>HClO2>HClO |
| D、热稳定性:NH3<H2O<HF<HCl |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com