
生活中常用一些化学知识,下列分析中正确的是 ( )
A. 医疗上可用硫酸钡作x射线透视肠胃的内服药,就是因为硫酸钡不溶于水
B. 氯气可用作消毒剂和漂白剂,是因为氯气与水反应生成的次氯酸具有强氧化性
C. 某雨水样品放置一段时间后pH由4.68变为4.28,是因为水中溶解的CO2增多
D. 加碘食盐中添加碘酸钾而不用碘化钾,是因为碘酸钾能溶于水而碘化钾不溶于水
 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源:2015-2016学年黑龙江省高一下期末化学试卷(解析版) 题型:选择题
下列反应中,原子利用率最高的是( )
A、CH4+Cl2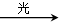 CH3Cl+HCl
CH3Cl+HCl
B、乙烯的燃烧:CH2=CH2+3O2 2CO2+2H2O
2CO2+2H2O
C、Fe2O3+6HCl=2FeCl3+3H2O
D、Na2CO3+H2O+CO2=2NaHCO3
查看答案和解析>>
科目:高中化学 来源:2015-2016学年甘肃省高一下期末理科化学试卷(解析版) 题型:选择题
通常人们把拆开1 mol某化学键所消耗的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热。
化学键 | Si-O | Si-Cl | H-H | H-Cl | Si-Si | Si-C |
E(kJ·mol?1) | 460 | 360 | 436 | 431 | 176 | 347 |
工业上高纯硅可通过下列反应制取:SiCl4(g)+2H2(g) Si(s)+4HCl(g),(已知1mol晶体Si中有2molSi-Si键),该反应的产生的热量为( )
Si(s)+4HCl(g),(已知1mol晶体Si中有2molSi-Si键),该反应的产生的热量为( )
A.吸收412 kJ·mol-1 B.放出412 kJ·mol-1
C.吸收236 kJ·mol-1 D.放出236 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省高一下期末化学试卷(解析版) 题型:填空题
X、Y、Z是短周期三种元素,它们在周期表中的位置如图所示。试回答:
|
| X |
| Y |
|
Z |
|
|
(1)X元素单质的化学式是__________________________________。
(2)Z元素的原子结构示意图为________________________________。
(3)Y在元素周期表中的位置是______________________。
(4)与Z同主族的下一周期元素的原子序数是________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省高一下期末化学试卷(解析版) 题型:选择题
下述实验能达到预期目的的是( )
编号 | 实验内容 | 实验目的 |
A | 将Na2CO3和NaHCO3 的固体混合物加热灼烧 | 除去NaHCO3中的Na2CO3 |
B | 常温时将CO通过装有SiO2 的硬质玻璃管 | 制取粗硅 |
C | 向新制得的K2S溶液中滴加新制的氯水 | 比较氯与硫的得电子能力 |
D | 分别向2支盛有冷水的试管中加入相同大小的镁条和铝条。 | 比较镁铝的金属性强弱 |
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省高一下期末化学试卷(解析版) 题型:选择题
某溶液中含有大量的Cl一、Br一、I一,若向l L该混合溶液中通入一定量的Cl2,溶液中Cl-、Br一、I一的物质的量与通入Cl2的体积(标准状况)的关系如下表所示,原溶液中Cl一、Br一、I一的物质的量浓度之比为( )
Cl2的体积(标准状况) | 5.6L | 11.2L | 22.4L |
n(C一)/mol | 1.5 | 2.0 | 3.0 |
n(Br一)/mol | 3.0 | 2.8 | 1.8 |
n(I一)/mol | x | 0 | 0 |
A、5:15:4 B、5:12:4 C、15 : 30 : 8 D、条件不足,无法计算
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省宿迁市高二下学期期末化学试卷(解析版) 题型:推断题
有机物A、B、C、D、E之间发生如下的转化:
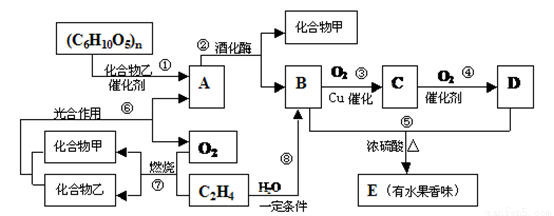
(1)写出D分子中官能团的名称: ,C物质的结构简式: 。
(2)上述①~⑧转化反应中,属于取代反应的有 ;属于加成反应的有 。(用反应序号填写)
(3)向A的水溶液中加入新制的Cu(OH)2并加热时产生的实验现象是 。
(4)请写出下列转化的化学反应方程式:
①(C6H10O5)n →A: ;
②B+D→E : ;
③乙烯生成聚乙烯: 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省宿迁市高二下学期期末化学试卷(解析版) 题型:选择题
下列措施一定能使反应速率加快的是
A.升高温度
B.加入生成物
C.缩小容器体积
D.增加反应物的物质的量
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高一下期末化学试卷(解析版) 题型:选择题
四种短周周期主族元素W、X、Y、Z的原子序数依次增大,W、X的简单离子具有相同电子层结构,X的原子半径是短周期主族元素原子中最大的,W与Y同族,Z与X形成的离子化合物中阴阳离子个数比为1:1。下列说法正确的是
A. 简单离子半径:W<X<Z
B. W与X形成的化合物溶于水后溶液呈碱性
C. 气态氢化物的热稳定性:W<Y
D. 最高价氧化物的水化物的酸性:Y>Z
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com