
| A. | 加热时间太短 | B. | 不应冷却后再加入AgNO3 | ||
| C. | 加AgNO3溶液前未用稀硝酸酸化 | D. | 反应后的溶液中不存在Cl- |
分析 1-氯乙烷中的氯元素不是以离子状态存在的,因此不能与AgNO3溶液直接反应,必须使之变为Cl-,反应后溶液显碱性,不能直接加AgNO3溶液,否则Ag+与OH-反应得到Ag2O黑色沉淀,影响氯的检验.
解答 解:1-氯乙烷中的氯元素不是以离子状态存在的,因此不能与AgNO3溶液直接反应,必须使之变为Cl-.因此,应通过1-氯乙烷在碱性溶液中水解得到,但要注意,反应后溶液显碱性,不能直接加AgNO3溶液,否则Ag+与OH-反应得到Ag2O黑色沉淀,影响氯的检验,所以应加入足量硝酸酸化后,再加AgNO3溶液检验.
故选C.
点评 本题考查氯离子的检验,题目难度中等,注意碱性条件下生成的AgOH不稳定,易分解生成Ag2O黑色沉淀而影响实验现象.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:填空题
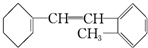 ,据此填写下列空格.
,据此填写下列空格.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②④ | C. | ①②③④ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
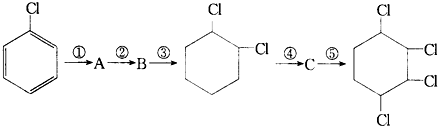
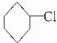 B
B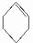
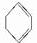 .
.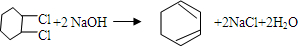 .
.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
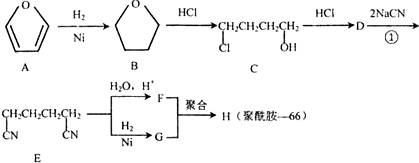
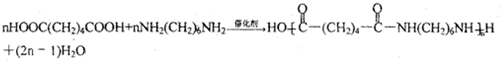 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 当lmol白磷转变成红磷时放出17kJ热量 | |
| B. | 当4g红磷转变成白磷时吸收17kJ热量 | |
| C. | 正反应是一个放热反应 | |
| D. | 白磷热稳定性比红磷大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com