

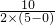 =1,故答案为:1;
=1,故答案为:1;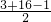 =9,根据硫酸根守恒确定H2SO4的化学计量数为9,再根据H元素守恒确定H2O的系数为9,故配平后方程式为:3KBrO3+16KI+9H2SO4=8I2+Br2+9K2SO4+KBr+9H2O,
=9,根据硫酸根守恒确定H2SO4的化学计量数为9,再根据H元素守恒确定H2O的系数为9,故配平后方程式为:3KBrO3+16KI+9H2SO4=8I2+Br2+9K2SO4+KBr+9H2O,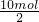 =5mol,故答案为:5mol.
=5mol,故答案为:5mol.

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| 阳离子 | H+、Na+、Al3+、Ag+、Ba2+ |
| 阴离子 | OH-、Cl-、CO32-、NO3-、SO42- |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源:学习周报 化学 人教课标高一版(必修1) 2009-2010学年 第9期 总第165期 人教课标版 题型:022
对于数以千万计的化学物质和种类繁多的化学反应,分类法的作用几乎是无可替代的.懂得物质的分类方法后,可以实现由“掌握一种物质”向“贯通一类物质”的转化,从而大大提高学习效率.
(1)现有下列五种物质:SO2、SiO2、CaO、MgO、Fe2O3、Na2O.按照不同的分类标准,它们中有一种物质与其他四种有着明显的不同,请找出该物质,并写出分类的依据.(至少要写出两种分类方法)
①________;②________.
(2)从反应有无离子参加,可以将化学反应分为离子反应和非离子反应.SO2与足量的NaOH溶液反应的离子方程式为________.从反应中________可以将化学反应分为氧化还原反应和非氧化还原反应.从上述氧化物中找出一种物质作为反应物,分别写一个非氧化还原反应和氧化还原反应的方程式(另外一种反应物任选,不需标明反应条件):________,________.
(3)虽然分类的方法不同,但离子反应和氧化还原反应之间也存在着一定的关系,请用简单的图示表示二者之间的关系:________.用离子反应方程式证明你的观点:________.
查看答案和解析>>
科目:高中化学 来源: 题型:
某氧化还原反应反应物和生成物如下:
27.请将下列五种物质:KBrO3、Br2 、I2 、KI、K2SO4分别填入下列横线上,组成一个未配平的化学方程式:
________+________+H2SO4 →_______+_______+______+KBr+H2O
28.该反应中的还原剂是 ,被还原的是元素是 (填写元素符号)。
29.如果该反应方程式中I2 和 KBr的系数为8和1,则
① Br2的系数是 ;
②请将反应物的化学式及配平后的系数填入下列空格,并标出电子转移方向和数目:
![]() __________ +
__________ + ![]() __________ +
__________ + ![]() H2SO4 →
H2SO4 →
30.反应物的配平系数可以发生变化,除了产物相对比例不同外,还有一个原因是:____________________________________________ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com