
| A. | 胶体中分散质粒子的直径大于溶液中分散质的粒子直径 | |
| B. | 向饱和的氯化铁溶液中加入氢氧化钠溶液得到红褐色沉淀 | |
| C. | 明矾【KAl(SO4)2•12H2O】可以做净水剂 | |
| D. | 氢氧化铁溶胶、稀豆浆、云雾等均具有丁达尔现象 |
分析 A.胶体区别于其他分散系的本质区别是防止微粒直径大小;
B.氯化铁溶液与氢氧化钠溶液发生复分解反应,产生红褐色沉淀;
C.明矾溶解溶液中铝离子水解生成氢氧化铝胶体,可以净水;
D.胶体能发生丁达尔现象.
解答 解:A.胶体中分散质粒子的直径大于溶液中分散质的粒子直径,和胶体知识有关,故A不符合;
B.氯化铁溶液与氢氧化钠溶液发生复分解反应FeCl3+3NaOH=Fe(OH)3↓+3NaCl,产生红褐色沉淀,与胶体性质无关,故B符合;
C.明矾溶解溶液中铝离子水解生成氢氧化铝胶体具有较大表面积,能吸附悬浮杂质净水,与胶体性质有关,故C不符合;
D.氢氧化铁溶胶、稀豆浆、云雾等是胶体,均具有丁达尔现象,与胶体性质无关,故D不符合;
故选B.
点评 本题考查胶体的性质,注意掌握胶体的性质是解题的关键,题目难度不大.


科目:高中化学 来源: 题型:解答题
| 实验序号 | 金属质量/g | 金属状态 | c(H2SO4) /mol•L-1 | V(H2SO4)/mL | 溶液温度/℃ | 金属消失的时间/s | |
| 反应前 | 反应后 | ||||||
| 1 | 0.10 | 丝 | 0.5 | 50 | 20 | 34 | 500 |
| 2 | 0.10 | 粉末 | 0.5 | 50 | 20 | 35 | 50 |
| 3 | 0.10 | 丝 | 1.0 | 50 | 20 | 35 | 125 |
| 4 | 0.10 | 丝 | 1.0 | 50 | 35 | 50 | 50 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 阳极 | 阴极 | 溶液甲 | 物质乙 | |
| A | Pt | Pt | NaOH | NaOH固体 |
| B | Pt | Pt | H2SO4 | H2O |
| C | Pt | Pt | NaCl | NaOH |
| D | 粗铜 | 精铜 | CuSO4 | Cu(OH)2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
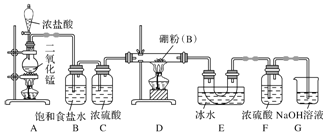
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学反应中的能量变化只体现为热量的形式 | |
| B. | 铝与氧化铁反应既是氧化还原反应,又是吸热反应[ | |
| C. | 甲烷燃烧反应过程中,旧键断裂吸收的能量小于新键形成释放的能量 | |
| D. | 外界条件相同时,放热反应的速率一定大于吸热反应的速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯可作催熟剂,其产量通常是衡量一个国家石油化工发展水平的标志 | |
| B. | 氯乙烯可用来制PVC塑料,PVC塑料可用作食品包装袋 | |
| C. | 卤代烃广泛应用于化工、药物生产及日常生活中,许多有机化合物都需要通过卤代烃去合成 | |
| D. | 苯有毒、有腐蚀性,不能用作提取食用油的有机溶剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com