
| A、软脂酸和硬脂酸 |
| B、甲酸甲酯和乙酸 |
| C、油酸和乙酸 |
| D、对甲基苯酚和苯甲醇 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙烯和聚乙烯都能与溴的四氯化碳溶液发生加成反应 |
| B、蔗糖和麦芽糖的水解产物都是葡萄糖 |
| C、石油经过分馏得到的各种产物是不同温度范围内的混合物 |
| D、苯和苯乙烯的最简式相同,是同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
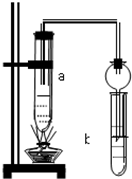 如图所示,在试管a中先加2mL乙醇,边摇动边缓缓加入5mL浓硫酸,摇匀冷却后,再加入2g无水醋酸钠,充分搅动后,固定在铁架台上.在试管b中加入适量的饱和Na2CO3溶液.连接好装置,给a加热,当观察到试管b中有明显现象时,停止实验.
如图所示,在试管a中先加2mL乙醇,边摇动边缓缓加入5mL浓硫酸,摇匀冷却后,再加入2g无水醋酸钠,充分搅动后,固定在铁架台上.在试管b中加入适量的饱和Na2CO3溶液.连接好装置,给a加热,当观察到试管b中有明显现象时,停止实验.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、所用NaOH已潮解 |
| B、向容量瓶加水时不慎超过了刻度线 |
| C、向容量瓶加水时眼睛一直俯视液面 |
| D、转移NaOH溶液后的烧杯没有洗涤 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| t/min | 0 | 2 | 4 | 6 | 8 | 10 |
| n(HI)/mol | 0.180 | 0.164 | 0.152 | 0.144 | 0.140 | 0.140 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、只有①?? |
| B、只有①②?? |
| C、只有①②③?? |
| D、全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com