
 .
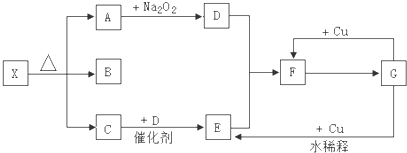
.分析 C能使湿润的红色石蕊试纸变蓝,应为NH3,A和过氧化钠反应生成D为气体,且A是无色气体,所以A应为CO2,D为O2,氨气和氧气在催化剂条件下加热生成NO和水,E能和氧气反应,所以E是NO,F为NO2,F和B反应生成G,G和铜反应生成二氧化氮,G为HNO3,B为液体,应为H2O,A、B、C的物质的量之比为1:1:1,则X为NH4HCO3,据此解答.
解答 解:C能使湿润的红色石蕊试纸变蓝,应为NH3,A和过氧化钠反应生成D为气体,且A是无色气体,所以A应为CO2,D为O2,氨气和氧气在催化剂条件下加热生成NO和水,E能和氧气反应,所以E是NO,F为NO2,F和B反应生成G,G和铜反应生成二氧化氮,G为HNO3,B为液体,应为H2O,A、B、C的物质的量之比为1:1:1,则X为NH4HCO3,
(1)由以上分析可知,B为H2O,F为NO2,
故答案为:H2O;NO2;
(2)A→D为Na2O2和CO2的反应,反应的化学方程式为:2CO2+2Na2O2═2Na2CO3+O2,反应中过氧化钠其氧化剂、还原剂作用,各占一半,故有1mol Na2O2完全反应,转移的电子数为:1mol×$\frac{1}{2}$×2×[(0-(-1)]=1mol,
故答案为:2CO2+2Na2O2═2Na2CO3+O2;1;
(3)G→E为稀硝酸和铜的反应,反应的化学方程式为:3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O,3个Cu原子完全反应失去6个电子,2个硝酸分子中的N原子得到6个电子生成NO气体,用双线桥标出电子转移的方向和数目为: ,
,
故答案为: ;
;
(4)将等物质的量的NO、NO2混合气通入NaOH溶液中,恰好被吸收,生成一种钠盐,令该盐中N元素化合价为x,根据电子转移守恒可知:x-2=4-x,解得x=3,故生成NaNO2,该反应的化学方程式为:NO+NO2+2NaOH═2NaNO2+H2O,
故答案为:NO+NO2+2NaOH═2NaNO2+H2O;
(5)实验室里,检验NH4HCO3中阳离子的方法是:取少量X于试管中,加入NaOH溶液,然后加热试管,再将湿润的红色石蕊试纸放在试管口,放出的气体能使湿润的红色石蕊试纸变蓝,则可说明其中有铵根离子,
故答案为:取少量X于试管中,加入NaOH溶液,然后加热试管,再将湿润的红色石蕊试纸放在试管口,放出的气体能使湿润的红色石蕊试纸变蓝,则可说明其中有铵根离子;
(6)120℃时,NH4HCO3完全分解生成NH3、H2O(气体)、CO2的物质的量之比为1:1:1,则混合产物的平均相对分子量=$\frac{79}{3}$=26.3,
故答案为:26.3.
点评 本题考查无机推断,题目难度中等,主要涉及N元素化合物性质及相互转化,“C能使湿润的红色石蕊试纸变蓝”为突破口,学习中注意相关基础知识的积累,试题有利于培养学生的分析、理解能力及逻辑推理能力.


 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案科目:高中化学 来源: 题型:选择题
| 选项 | X溶液 | 固体Y |  |
| A | 浓硫酸 | 铜粉 | |
| B | 浓氨水 | CaO | |
| C | 稀盐酸 | 石灰石 | |
| D | 浓盐酸 | 高锰酸钾 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验 | 现象 | 离子方程式 | |
| A | 苯酚钠溶液中通入少量CO2 | 产生白色浑浊 | 2C6H5O-+CO2+H2O→2C6H5OH+CO32- |
| B | 在少量稀碳酸钠溶液中逐滴加入稀盐酸至过量. | 开始无气泡,后来有气泡. | CO32-+H+→HCO3- HCO3-+H+→CO2↑+H2O |
| C | 将过量氯化铝溶液逐滴加入到氢氧化钠溶液中 | 先产生白色沉淀而后逐渐溶解 | Al3++3OH-→Al(OH)3↓ Al(OH)3+OH-→AlO2-+H2O |
| D | 向含有酚酞的氢氧化钡溶液中滴加稀硫酸 | 产生白色沉淀,溶液由红色变成无色. | Ba2++OH+H++SO42-→BaSO4↓+H2O |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO3的物质的量为4.5mol的状态为平衡状态 | |
| B. | O2的平均反应速率为0.4amol•(L•min)-1 | |
| C. | SO2和O2的反应百分率相等 | |
| D. | 达到化学平衡状态时容器内压强减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、SO42-、I-、NO3- | B. | Cu2+、Na+、Cl-、S2- | ||
| C. | Ca2+、K+、HCO3-、NO3- | D. | K+、Na+、CH3COO-、Br- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
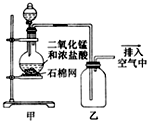
| A. | 该装置图中至少存在两处明显错误 | |
| B. | 烧瓶中的MnO2可换成KMnO4 | |
| C. | 在乙后连一盛有饱和食盐水的烧杯可进行尾气处理 | |
| D. | 在集气瓶的导管口处放一片湿润的淀粉碘化钾试纸可以证明是否有氯气逸出 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液中四种粒子之间满足:c(Cl-)>c(H+)>c(NH4+)>c(OH-) | |
| B. | 若溶液中粒子间满足:c(NH4+)>c(Cl-)>c(OH-)>c(H+),则溶液中溶质为:NH3•H2O和NH4Cl | |
| C. | 若溶液中粒子间满足:c(Cl-)>c(NH4+)>c(H+)>c(OH-),则溶液中溶质只有NH4Cl | |
| D. | 若溶液中c(NH4+)=c(Cl-),则该溶液pH等于7. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  某可逆反应的正反应是吸热反应 | B. |  等量的锌粉与足量的盐酸反应 | ||
| C. | 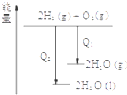 氯气和氧气反应中的能量变化 | D. |  气态氢化物沸点 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com