
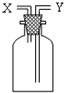
 ��ͼ��ʾ��װ����ʵ��������;�ȽϹ㷺��
��ͼ��ʾ��װ����ʵ��������;�ȽϹ㷺��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
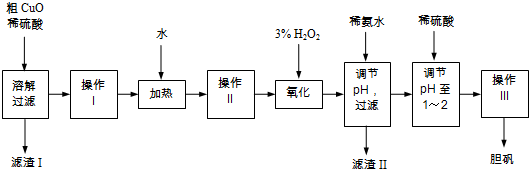
 ͭ���ʼ��仯�����ڹ�ҵ�����Ϳ���������Ҫ���ã�
ͭ���ʼ��仯�����ڹ�ҵ�����Ϳ���������Ҫ���ã�| �������� | Fe3+ | Fe2+ | Cu2+ |
| �������↑ʼ����ʱ��pH | 1.9 | 7.0 | 4.7 |
| ����������ȫ����ʱ��pH | 3.2 | 9.0 | 6.7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| Fe3+ | Fe2+ | Cu2+ | |
| ��ʼ����ʱ��pH | 2.7 | 7.6 | 5.2 |
| ��ȫ����ʱ��pH | 3.7 | 9.6 | 6.4 |
| ��һ��ʵ�� | �ڶ���ʵ�� | |
| ����������g�� | 14.520 | 14.670 |
| ��������+����������g�� | 17.020 | 18.350 |
| ��һ�μ��ȡ���ȴ��������g�� | 16.070 | 16.989 |
| �ڶ��μ��ȡ���ȴ��������g�� | 16.070 | 16.988 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ʵ��Ŀ�� | �Լ������� |
| ֤��Na2CO3��Һ���м��� | |
| ����Na2SO4��Һ�ͣ�NH4��2SO4��Һ | |
| ��������ˮ���Ƿ���Cl- | |
| ��ȥFeCl2��Һ��������FeCl3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| �� ���� |
IA | 0 | |||||||
| 1 | ��A | ��A | ��A | ��A | ��A | ��A | |||
| 2 | �� | �� | Ne | ||||||
| 3 | �� | �� | �� | �� | |||||
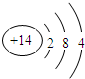
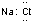
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| 1 |
| 2 |
| 1 |
| 2 |
| c(CO)-c(H2) |
| c(H2O) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Na2CO3 |
| B��HCl |
| C��Na2SO4 |
| D��KNO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����������ˮ��Ӧ��K+2H2O=K++2OH-+H2�� |
| B���Ȼ�����Һ����������Һ��Ӧ��Ag++Cl-=AgCl�� |
| C��������������ˮ��Ӧ��Cl2+H2O=2H++Cl-+ClO- |
| D����CuSO4��Һ�м������Ba��OH��2��Һ��Ba2++SO42-=BaSO4�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com