
| A、Mg2+、Fe2+、SO42- |
| B、Ba2+、NH4+、Br- |
| C、Al3+、HCO3-、Cl- |
| D、Na+、SiO32-、ClO- |


 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案科目:高中化学 来源: 题型:
| A、原氨水物质的量浓度为0.1 mol?L-1 |
| B、反应后的溶液中c(NH4+)+c(NH3?H2O)+c(NH3)=0.1 mol?L-1 |
| C、反应后的溶液中:c(Clˉ)>c(NH4+)>c(H+)>c(OHˉ) |
| D、原氨水中:c(NH4+)+c(H+)=c(OHˉ) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、16g02和O3的混合气体所含氧原子数在NA/3到NA/2之间 |
| B、62g Na2O与78gNa202含有的离子数均为3NA |
| C、1molC5H12含共价键数为20NA |
| D、1LO.lmol/L的醋酸溶液中所含离子总数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、滴人甲基橙显红色的溶液中:NH4+、Ba2+、AlO-2、Cl- | ||||
B、Kw/c(H+)=0.1 mol/L的溶液:Na+、K+、Si
| ||||
C、含有较多S
| ||||
D、澄清透明溶液中:K+、Mn
|
查看答案和解析>>
科目:高中化学 来源: 题型:
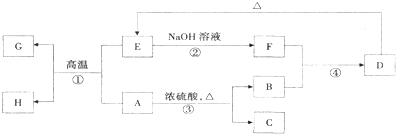
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、蓝色沉淀为Cu(OH)2,深蓝色溶液中所含Cu2+浓度较大 |
| B、白色沉淀为+2价铜的某种亚硫酸盐,溶于H2SO4发生复分解反应 |
| C、白色沉淀为+1价铜的某种亚硫酸盐,在酸性条件下发生了氧化还原反应 |
| D、反应过程中消耗的SO2与生成的SO2的物相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、9gD2O中含有的质子数为5NA |
| B、1molCaCl2中含有的离子数为3NA |
| C、30g甲醛中含共用电子对总数为4NA |
| D、71gCl2与足量NaOH溶液反应转移的电子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、pH=0的溶液中:Fe3+、Mg2+、Cl-、SO42- |
| B、水电离出的c(H+)=1×10-13mol/L的溶液中:K+、HCO3-、Cl-、S2- |
| C、使紫色石蕊试液显蓝色的溶液中:Mg2+、NO3-、Fe3+、SO42- |
| D、溶有碳酸氢钠的溶液:K+、SO42-、Cl-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
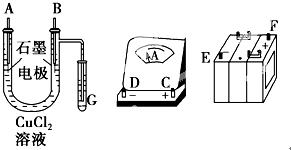 某学生试图用电解法根据电极上析出物质的质量来验证阿伏加德罗常数值,其实验方案的要点为:
某学生试图用电解法根据电极上析出物质的质量来验证阿伏加德罗常数值,其实验方案的要点为:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com