
| A. | ①②③④ | B. | ①③④⑤ | C. | ②④⑤ | D. | ①②③④⑤ |
分析 据氯气先氧化碘离子,然后氧化二价铁,最后氧化溴离子,向反应后的溶液中滴加KSCN溶液,结果溶液变为红色,说明含有铁离子,则碘离子全部被氧化,二价铁部分或全部被氧化,溴离子可能被氧化来分析.
解答 解:氯气先氧化碘离子,然后氧化二价铁,最后氧化溴离子,向反应后的溶液中滴加KSCN溶液,结果溶液变为红色,说明碘离子全部被氧化,二价铁部分或全部被氧化,溴离子可能被氧化,
①氯气先氧化碘离子,然后氧化二价铁,最后氧化溴离子,则碘离子还原性最强,溴离子最弱,则还原性:I-、Fe2+、Br-的顺序逐渐减弱,故正确;
②原溶液中的Br-可能被氧化,也可能未被氧化,故错误;
③通入氯气之后原溶液中的二价铁部分或全部被氧化,故正确;
④通入氯气之后原溶液中的二价铁部分或全部被氧化,所以不能确定通入氯气之后的溶液中是否存在Fe2+,故正确;
⑤若取少量所得溶液,再加入CCl4溶液,静置、分液,向上层溶液中加入足量的AgNO3溶液,只产生白色沉淀,说明原溶液中的Br-被完全氧化,I-、Fe2+均被完全氧化,故正确;
故选B.
点评 本题考查学生氧化还原反应中氧化性和还原性强弱的知识,题目难度不大,侧重于氧化还原反应在离子反应中应用的考查.


科目:高中化学 来源: 题型:选择题
| A. | 1:1 | B. | 2:3 | C. | 3:4 | D. | 4:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
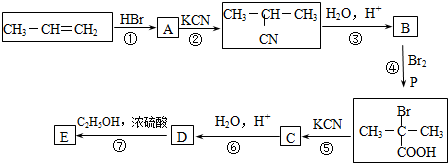

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
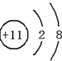 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
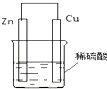 能源是人类生活和社会发展的基础,研究化学反应中的能量变化,有助于更好地利用化学反应为生产和生活服务.阅读下列有关能源的材料,回答有关问题:
能源是人类生活和社会发展的基础,研究化学反应中的能量变化,有助于更好地利用化学反应为生产和生活服务.阅读下列有关能源的材料,回答有关问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
. ,A2C的结构式:H-O-H.
,A2C的结构式:H-O-H. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| A | 原子半径最小 |
| B | 核外3个能级上的电子数相等 |
| C | 其氢化物的沸点比同族相邻周期元素氢化物的沸点高 |
| D | 2p轨道上成对电子数与未成对电子数相等 |
| E | N层电子数为1,内层轨道全部排满电子 |
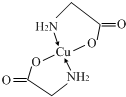 .
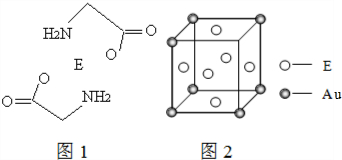
.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com