
中学常见的某反应的化学方程式为A+B―→C+D+H2O(未配平,反应条件略去)。请回答下列有关问题:
(1)若A是铁,B是稀硝酸(过量),且A可溶于C溶液中。则A与B反应的离子方程式为________________________________________________________________________。
(2)若C、D均为气体,且都能使澄清石灰水变浑浊,则上述反应的化学方程式为________________________________________________________________________。
(3)若C是无色刺激性气味的气体,其水溶液呈弱碱性,C能发生催化氧化反应。写出该反应的化学方程式_______________________________________________________
________________________________________________________________________。
(4)若D为氯碱工业的主要原料,C是造成温室效应的主要气体之一,则上述反应的化学方程式
________________________________________________________________________。
科目:高中化学 来源: 题型:
4,7二甲基香豆素(熔点132.6 ℃)是一种重要的香料,广泛分布于植物界中,以间甲苯酚为原料的合成反应如下:

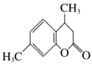 +C2H5OH+H2O
+C2H5OH+H2O
4,7二甲基香豆素
实验装置图如下:

主要实验步骤:
步骤1:向三颈烧瓶中加入60 mL浓硫酸,并冷却至0 ℃以下,边搅拌边滴入间甲苯酚30 mL(0.29 mol)和乙酰乙酸乙酯26.4 mL(0.21 mol)的混合物。
步骤2:保持在10 ℃下,搅拌12 h,反应完全后,将其倒入冰水混合物中,然后抽滤、水洗得粗品。
步骤3:粗品用乙醇溶解并重结晶,得白色针状晶体并烘干,称得产品质量为33.0 g。
(1)图中仪器名称:a____________,b____________。
(2)浓H2SO4需要冷却至0 ℃以下的原因是____________________________________
________________________________________________________________________。
(3)反应需要搅拌12 h,其原因是___________________________________________
________________________________________________________________________。
(4)确定最终产品是4,7二甲基香豆素的实验或方法是____________________。
(5)本次实验产率为____________。
答案 (1)恒压滴液漏斗 吸滤瓶
(2)防止浓硫酸将有机物氧化和炭化
(3)使反应物充分接触,提高反应速率
(4)测量熔点或测定其红外(紫外)光谱(及核磁共振氢谱)等 (5)89%
查看答案和解析>>
科目:高中化学 来源: 题型:
在常温下向盛满水并倒置于水槽中的试管里先后通入4 mL NO2、4 mL NO、5 mL O2,经过一段时间后,试管里剩余的气体有( )
A.NO B.O2
C.NO2和O2 D.NO和O2
查看答案和解析>>
科目:高中化学 来源: 题型:
6.4 g铜与过量的硝酸(8 mol·L-1 60 mL)充分反应后,硝酸的还原产物有NO、NO2,反应后溶液中含H+为n mol,此时溶液中含NO3-的物质的量为( )
A.0.28 mol B.0.31 mol
C.(n+0.2) mol D.(n+0.4)mol
查看答案和解析>>
科目:高中化学 来源: 题型:
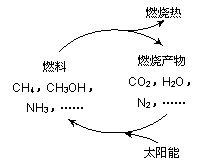
能源是当今社会发展的三大支柱之一。有专家提出:如果对燃料燃烧产物如CO2、H2O、N2等能够实现利用太阳能让它们重新组合(如右图),可以节约燃料,缓解能源危机。在此构想的物质循环中太阳能最终转化为
A.化学能 B.热能 C.生物能 D.电能
查看答案和解析>>
科目:高中化学 来源: 题型:
二氧化氮存在下列平衡:2NO2(g) N2O4(g) ∆H< 0,在测定NO2的相对分子质量时,下列条件中较为适宜的是
A.温度130℃、压强3.03×105Pa B.温度25℃、压强1.01×105Pa
C.温度130℃、压强5.05×104Pa D.温度0℃、压强5.05×104Pa
查看答案和解析>>
科目:高中化学 来源: 题型:
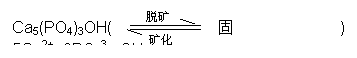 牙齿表面由一层硬的、组成为Ca5(PO4)3OH的物质保护着,它在唾液中存在下列平衡:
牙齿表面由一层硬的、组成为Ca5(PO4)3OH的物质保护着,它在唾液中存在下列平衡:
进食后,细菌和酶作用于食物,产生有机酸,这时牙齿就会受到腐蚀,其原因是__________________________________。已知Ca5(PO4)3F(固)的溶解度比上面的矿化产物更小,质地更坚固。当牙膏中配有氟化物添加剂后能防止龋齿的原因:_________________________,根据以上原理,请你提出一种在牙膏配方中其它能促进矿化的方法:______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
将40克NaOH溶于水中,配制成1L溶液,则该溶液的物质的量浓度为
0.1mol/L B. 0.5mol/L C. 4mol/L D. 1mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com