
已知水和苯互不相溶,苯不与钠反应,在烧杯中加水和苯(密度:0.88g/cm3)各50mL.将一小粒金属钠(密度:0.97g/cm3)投入烧杯中,观察到的现象可能是()
| A. | 钠在水层中反应并四处游动 | |
| B. | 钠停留在苯层中不发生反应 | |
| C. | 钠在苯的液面上反应并四处游动 | |
| D. | 钠在苯与水的界面处反应并可能做上、下跳动 |
科目:高中化学 来源: 题型:
下列说法中正确的是 ( )
A.所有主族元素的正化合价数,等于它的族序数
B.第ⅦA族元素的原子随核电荷数的增加,得电子能力逐渐减弱
C.第ⅠA、第ⅡA族元素的阳离子与同周期稀有气体元素的原子具有相同的核外电子排布
D.前三周期元素中共有非金属元素12种
查看答案和解析>>
科目:高中化学 来源: 题型:
)下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用元素符号或化学用语回答下列问题:
| 族 周期 | IA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ||||||
| 3 | ④ | ⑤ | ⑥ | ⑦ |
(1)①和②形成的最简单有机化合物分子的结构式为_____________。
(2)下列事实能证明②的非金属性比⑥强的是
|
|
 O3+CO2↑
O3+CO2↑ B. SiO2+2C ==== Si+2CO↑
C. Na2SiO3+CO2+2H2O=H2SiO3↓+Na2CO3
D.CH4比SiH4稳定
(3)写出①、③、④三种元素组成化合物的电子式___________。
(4)③、④、⑤所形成的简单离 子半径由大到小的顺序:___ ________。
子半径由大到小的顺序:___ ________。
(5)①、②、⑦三种元素按原子个数之比为11︰5︰1组成的有机化合物中含有两个-CH3的同分异构体有
种。
(6) 最近科学家制造了一种燃料电池,一个电极通入空气,另一电极通入液化石油气(以C4H10表示).电池的电解质是掺杂了Y2O3的ZrO2晶体,它在高温下能传导O2-.已知该电池的负极反应为:
C4H10+13O2--26e-===4CO2+5H2O,则该电池的正极反应为_____________________,电池工作时,电池中O2-向________极移动.
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液中有关物质的量浓度关系正确的是 ( )
A. pH = 2 的HA溶液与pH=12的MOH溶液任意比混合
c(H+) + c(M+)=c(A-) + c(OH-)
B. pH相等的CH3COONa、NaOH和NaCO3三种溶液:
c(NaOH) < c(CH3COONa) < c(NaCO3)
C. 物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合
c(CH3COO-) + 2c(OH-) = 2c(H+) + c(CH3COOH)
D. 0.1mol·L-1的NaHA溶液,其pH = 4:c(HA-)>c(H+)>c(H2A)>c(A2-)
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上制备氯化铜时,是将浓盐酸用水蒸汽加热至80℃左右,慢慢加入粗制氧化铜粉(含杂质氧化亚铁),充分搅拌,使之溶解,反应如下:
CuO + 2HCl = CuCl2 + H2O ,FeO + 2HCl = FeCl2 + H2O。
已知:pH≥9.6时,Fe2+以Fe(OH)2的形式完全沉淀;
pH≥4.4时,Cu2+以Cu(OH)2的形式开始沉淀; pH≥6.4时,Cu2+以Cu(OH)2的形式完全沉淀;pH在3~4时,Fe3+以Fe(OH)3的形式完全沉淀。
⑴为除去溶液中F e2+,可采用的方法是 。
e2+,可采用的方法是 。
⑵工业上为除去溶液中的Fe2+,常 使用NaClO,当向溶液中加入NaClO后,可能发生反应的离子方程式
使用NaClO,当向溶液中加入NaClO后,可能发生反应的离子方程式 为_____________________________________________________。溶液的pH变化是 。
为_____________________________________________________。溶液的pH变化是 。
⑶若此溶液只含Fe3+时,要调整pH在3~4之间,此时最好向溶液中加入 。
(4)已知溶液中c(Cu2+)与溶液pH的关系为lg c(Cu2+)=8.6-2pH,若溶液中c(Cu2+)为1 mol/L,要保证此溶液中Cu2+刚好不发生Cu(OH)2沉淀,则溶液pH应为___________,此时溶液中的铁离子能否沉淀完全______ ___(填“能”或“否”)。
___(填“能”或“否”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
Na2CO3固体中可能含有杂质K2CO3、NaHCO3、NaCl中一种或几种,取10.6g样品,加入足量的稀盐酸产生气体4.8g,下列分析正确的是()
| A. | 一定含有NaHCO3 | B. | 一定含有K2CO3 | |
| C. | 一定不含NaCl | D. | 一定含有NaCl |
查看答案和解析>>
科目:高中化学 来源: 题型:
有无色溶液,加入Na2O2时有无色无味气体放出,并有白色沉淀生成,加入Na2O2的量与生成白色沉淀的量如图所示.该无色溶液中含有的物质是()
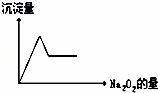
| A. | CaCl2和MgCl2、 | B. | Al2 (SO4)3 | |
| C. | Al2(SO4)3和MgSO4 | D. | Na2SO4和MgSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
根据下表中部分短周期元素的原子半径及主要化合价信息:
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.130 | 0.118 | 0.090 | 0.102 | 0.073 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
请判断以下叙述正确的是( )
A.氢化物的沸点为H2T<H2R B. L2+与R2-的核外电子数相等
C.与稀盐酸反应单质Q比单质L快 D.M与T形成的化合物具有两性
查看答案和解析>>
科目:高中化学 来源: 题型:
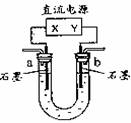
用右图装置(X、Y是直流电源的两极)分别进行下列各组实验,则下表中所列各项对应关系均正确的一组是 ( )
| 选项 | 电源X极 | 实验前U形管中液体 | 通电后现象及结论 |
| A | 正极 | Na2SO4溶液 | U形管两端滴入酚酞后, a管中呈红色 |
| B | 正极 | AgNO3溶液 | b管中电极反应式是4OH—4e-=2H2O+O2↑ |
| C | 负极 | KCl和CuCl2混合溶液 | 相同条件下,a、b两管中产生的气体总体积可能相等 |
| D | 负极 | AlCl3溶液 | a管中先产生白色沉淀后沉淀溶解 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com