
苹果醋(ACV)是一种由苹果发酵而成的酸性饮品,具有解毒.降脂等药效,主要酸性物质为苹果酸.苹果酸在分离提纯后的化学分析如下:①相对分子质量不超过150,完全燃烧后只生成CO2和H2O,分子中C、H质量分数分别为w(C)=35.82%.w(H)=4.48%;②1mol该酸与足量的NaHCO3反应放出44.8L CO2,与足量的Na反应放出33.6L H2(气体体积均已折算为标准状况);(已知:RCOOH+NaHCO3→RCOONa+CO2+H2O,2RCOOH+2Na→2RCOONa+H2,2ROH+2Na→2RONa+H2③该分子中存在四种化学环境不同的碳原子,氢原子处于五种不同的化学环境.回答下列问题:
(1)苹果酸的分子式为 ,分子中有 个羧基.
(2)写出苹果酸的结构简式 .
(3)若一个碳上边有四个不同的基团,就可以认为是手性碳原子,在苹果酸的结构简式中是否存在手性碳原子,若有请用*符号标出.标在(2)小题上.
| 有机物的推断. | |
| 专题: | 有机物的化学性质及推断. |
| 分析: | (1)苹果酸分子中w(C)=35.82%,w(H)=4.48%,则O的质量分数为1﹣35.82%﹣4.48%=59.7%,相对分子质量不超过150,则O原子最大数目= (2)苹果酸分子含有2个﹣COOH、1个﹣OH,该分子中存在四种化学环境不同的碳原子,氢原子处于五种不同的化学环境,结合分子式书写其结构简式; (3)根据(2)中苹果酸的结构简式进行判断. |
| 解答: | 解:(1)苹果酸分子中w(C)=35.82%,w(H)=4.48%,则O的质量分数为1﹣35.82%﹣4.48%=59.7%,相对分子质量不超过150,则O原子最大数目= 故答案为:C4H6O5;2; (2)苹果酸的分子式为C4H6O5,苹果酸分子含有2个﹣COOH、1个﹣OH,该分子中存在四种化学环境不同的碳原子,氢原子处于五种不同的化学环境,则苹果酸的结构简式为 (3)苹果酸的结构简式为 |
| 点评: | 本题考查有机物的推断,属于计算型推断,确定分子含有O原子数目是关键,需要学生熟练掌握醇、羧酸的性质,题目难度中等. |


科目:高中化学 来源: 题型:
某化学实验小组的同学用下列仪器组装两套完全相同的装置,定量探究浓度对反应速率的影响。
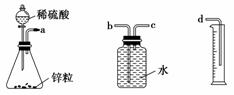
(1)为达到本实验的目的,其装置连接顺序为a连________,________连________。
(2)连接好装置后的下一步操作是__________________________________________________________。
(3)锥形瓶中发生反应的离子方程式为__________________________________________________________。
(4)两套装置的分液漏斗所装的试剂分别为1 mol·L-1硫酸和4 mol·L-1硫酸,该小组同学要测定并记录的数据如下表:
| 加入的试剂 | H2的体积(相同条件下) | 反应时间 | 反应速率 |
| 1 mol·L-1硫酸 | 10 mL | t1 | v1 |
| 4 mol·L-1硫酸 | 10 mL | t2 | v2 |
该小组同学通过实验得到的结果是:v1小于v2,其定量依据是________。
(5)另有一组同学测定了每隔一分钟,锥形瓶中硫酸的浓度,记录结果如下:
| 时间(min) | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 硫酸浓度(mol·L-1) | 4.0 | 3.8 | 3.5 | 3.1 | 2.6 | 2.2 | 1.9 | 1.8 | … |
请在给定的坐标图中作出v(H2)-t的图像。
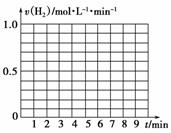
请解释0到4 min时该化学反应速率随时间变化的原因:__________________________________________________________
__________________________________________________________。
(6)除上述实验方案可定量测定该反应的化学反应速率外,还可能有的实验测定方法有:__________________________________________________________
__________________________________________________________。(任写一种)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于芳香烃的叙述正确的是( )
|
| A. | 其组成的通式是CnH2n﹣6 |
|
| B. | 分子中含有苯环的有机物 |
|
| C. | 分子中含有苯环的碳氢化合物 |
|
| D. | 苯及其同系物的总称 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某烃的结构简式为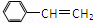 ,它可能具有的性质是( )
,它可能具有的性质是( )
|
| A. | 能使溴水褪色,但不能使酸性KMnO4溶液褪色 |
|
| B. | 与足量氢气反应生成苯乙烷 |
|
| C. | 能发生加聚反应,生成物可用表示 |
|
| D. | 易溶于水,也易溶于有机溶剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
①用一种试剂将下列各组物质鉴别开.
(1) 和
和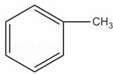 :
:
(2) ,
, 和C6H12(已烯):
和C6H12(已烯):
(3)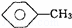 ,CCl4和乙醇
,CCl4和乙醇
②填写
(1)CH3COOC2H5中含有官能团的名称:
(2)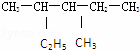 的系统命名:
的系统命名:
(3)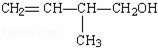 的键线式: .
的键线式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下,4个容积均为1 L的容器中,分别进行反应:C(s)+H2O(g)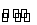 CO(g)+H2(g) ΔH=+131.3 kJ·mol-1[各容器中C(s)均足量],在某时刻测得有关物质的浓度及
CO(g)+H2(g) ΔH=+131.3 kJ·mol-1[各容器中C(s)均足量],在某时刻测得有关物质的浓度及 正、逆反应速率的关系如
正、逆反应速率的关系如 下表。下列说法正确的是( )
下表。下列说法正确的是( )

A.在容器Ⅱ中,v(正)<v(逆)
B.在容器Ⅳ中,再加入少量C,反应速率加快
C.在容器Ⅲ中, 反应达到平衡时要吸收热量
D.若将平衡时容器Ⅰ、Ⅳ中的物质混合于容积为1 L的容器中,则反应仍处于 平衡状态
平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
“玉兔”号月球车用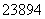 Pu作为热源材料,下列关于
Pu作为热源材料,下列关于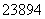 Pu的说法正确的是( )
Pu的说法正确的是( )
A.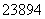 Pu与
Pu与 U互为同位素
U互为同位素
B.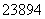 Pu与
Pu与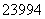 Pu互为同素异形体
Pu互为同素异形体
C.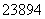 Pu与
Pu与 U具有完全相同的化学性质
U具有完全相同的化学性质
D.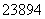 Pu与
Pu与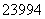 Pu具有相同的最外层电子
Pu具有相同的最外层电子
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期主族元素X、Y、Z、W的原子序数依次增大。X原子的最外层电子数是其内层电子数的2倍,Y是地壳中含量最高的元素,Z2+与Y2-具有相同的电子层结构,W与X同主族。下列说法正确的是( )
A.原子半径的大小顺序:r(W)>r(Z)>r(Y)>r(X)
B.Y分别与Z、W形成的化合物中化学键类型相同
C.X的最高价氧化物对应的水化物的酸性比W的弱
D.Y的气态简单氢化物的热稳定性比W的强
查看答案和解析>>
科目:高中化学 来源: 题型:
下列对各组离子或物质是否能够大量共存解释正确的是(双选)( )
| A | 常温常压下NH3、O2、H2、CO2 | 不能 |
| 共存 | NH3为碱性气体、CO2为酸性气体,二者反应生成(NH4)2CO3 | |
| B | c(OH-)=1.0×10-13 mol·L-1溶液中,Fe2+、NO | 不能 |
| 共存 | 发生反应:3Fe2++NO | |
| C | 溶液中:K+、Cu2+、Cl-、NH3·H2O | 不能 |
| 共存 | 发生反应:Cu2++2NH3·H2O===Cu(OH)2↓+2NH | |
| D | 溶液中:Al3+、Na+、SO | 可以 |
| 共存 | 不能发生反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com