
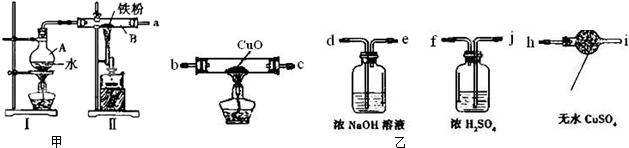
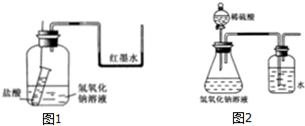
分析 (1)图甲为铁与水蒸气反应的实验装置,生成的水蒸气和铁在高温下反应需要装置气密性完好;
(2)硬质玻璃管B内所发生反应是铁和水蒸气反应生成四氧化三铁和氢气;
(3)为了验证硬质玻璃管B中反应后的气体产物是H2,同时含有水蒸气,需要通过装置中的浓硫酸干燥氢气,然后通过装置中的氧化铜发生氧化还原反应生成红色铜和水蒸气,通过无水硫酸铜检验生成的水蒸气存在,最后需要剩余氢气的处理;
(4)反应后,将图甲II装置中硬质玻璃管B内的全部固体置于试管中,加入60mL1mol/L的稀盐酸,固体恰好完全溶解,再滴加KSCN溶液,发现溶液不显血红色,说明无铁离子存在,四氧化三铁溶解后生成亚铁离子和铁离子,说明过量的铁和过量的盐酸反应生成氯化亚铁和氢气,铁离子反应生成亚铁离子,反应后全部生成氯化亚铁,结合元素守恒计算铁粉质量;
解答 解:(1)铁与水蒸气反应的实验装置分析可知,装置中A需要生成水蒸气,通入B中和铁在高温下反应所以需要装置气密性完好,实验前应先进行的操作是检查装置气密性,
故答案为:检查装置气密性;
(2)图甲I为产生水蒸气的装置,图甲II为铁与水蒸气反应的装置,硬质玻璃管B内所发生反应是铁和水蒸气反应生成四氧化三铁和氢气,反应的化学方程式为:3Fe+4H2O$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2,
故答案为:3Fe+4H2O$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2;
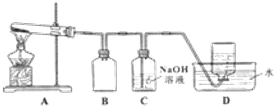
(3)硬质玻璃管B中反应后的气体产物是H2,同时含有水蒸气,需要通过装置中的浓硫酸干燥氢气,然后通过装置中的氧化铜发生氧化还原反应生成红色铜和水蒸气,通过无水硫酸铜检验生成的水蒸气存在,最后需要剩余氢气的处理,为了验证硬质玻璃管B中反应后的气体产物是H2,其连接顺序为ajfbch,
故答案为:jfbch;
(4)反应后,将图甲II装置中硬质玻璃管B内的全部固体置于试管中,加入60mL1mol/L的稀盐酸,固体恰好完全溶解,再滴加KSCN溶液,发现溶液不显血红色,说明无铁离子存在,四氧化三铁溶解后生成亚铁离子和铁离子,反应的离子方程式为:Fe3O4+8H+=Fe2++2Fe3++4H2O,过量的铁和过量的盐酸反应生成氯化亚铁和氢气,反应的离子方程式为:Fe+2H+=Fe2++H2↑,铁离子反应生成亚铁离子,反应的离子方程式为:Fe+2Fe3+=3Fe2+,依据元素元素守恒计算,铁元素来源于铁单质,氯元素来源于盐酸溶液中的氯化氢,
FeCl2~2HCl~Fe,
2 1
0.060L×1mol/L n=0.03mol
反应前硬质玻璃管B中加入Fe粉的质量=56g/mol×0.03mol=1.68g,
故答案为:Fe3O4+8H+=Fe2++2Fe3++4H2O、Fe+2H+=Fe2++H2↑、Fe+2Fe3+=3Fe2+;1.68.
点评 本题考查了物质制备、物质性质、反应产物的实验验证等知识点,掌握基础是解题关键,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
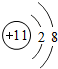 ;
;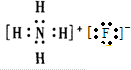 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 操作 | 现象 | 结论 |
| 取少量除尽Ag+后的溶液于试管中,加入KSCN溶液,振荡 | 变成血红色 | 存在Fe3+ |
| 取少量除尽Ag+后的溶液于试管中,加入K3[Fe(CN)6],振荡 | 产生蓝色沉淀 | 存在Fe2+ |
| 实验编号 | 操作 | 现象 |
| a | 加入足量氨水,振荡 | 黑色固体不溶解 |
| b | 加入足量稀硫酸,振荡 | 黑色固体溶解,并有气体产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 14g N2和32g O2 | B. | 34g NH3 和4g H2 | ||
| C. | 2LCO2和2LH2O | D. | 11.2LO2和0.5molO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 20Ne和22Ne互为同位素 | B. | 20Ne和22Ne互为同素异形体 | ||
| C. | 20Ne和22Ne的质量数相同 | D. | 20Ne和22Ne的中子数相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com