
分析 (1)当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态;
(2)该反应是一个反应前后气体体积减小的放热反应,欲提高SO2的转化率,则改变条件使平衡向正反应方向移动;
(3)混合气体通过过量NaOH溶液时,减少的气体是二氧化硫和三氧化硫,根据剩余氧气的量计算参加反应的氧气的量,根据参加反应的氧气的量计算参加反应的二氧化硫、三氧化硫的量,二氧化硫和三氧化硫混合气体体积减去三氧化硫的量就是未参加反应的二氧化硫的量,再根据转化率公式计算;
(4)平衡混合气体5%通过氯化钡溶液只吸收三氧化硫,二氧化硫不能生成沉淀,依据三氧化硫物质的量计算生成硫酸钡沉淀质量.
解答 解:(1)a.可逆反应到达平衡时SO2和SO3浓度不一定相等,与二氧化硫的起始浓度以及转化率有关,故a错误;
b.可逆反应达到平衡状态时,各物质的百分含量不变,SO2百分含量保持不变,说明到达平衡状态,故b正确;
c.随反应进行气体的物质的量减小,恒温恒容下,容器内气体压强减小,当容器中气体的压强不变,说明到达平衡状态,故c正确;
d.SO3的生成速率与SO2的消耗速率都表示正反应速率,反应始终二者都按1:1进行,不能说明到达平衡状态,故d错误;
e.混合气体的质量不变,容器的体积不变,所以密度始终不变,不能说明到达平衡状态,故f错误;
故选bc,
故答案为:bc;
(2)a.向装置中再充入N2,反应物和生成物的浓度不变,平衡不移动,所以不能提高转化率,故a错误;
b.向装置中再充入O2,氧气浓度增大,平衡向正反应方向移动,提高了二氧化硫的转化率,故b正确;
c.改变反应的催化剂只改变反应速率,不改变平衡,所以不能提高二氧化硫的转化率,故c错误;
d.升高温度,平衡向逆反应方向移动,降低了二氧化硫的转化率,故d错误;
故选b
故答案为:b;
(3)混合气体通过过量NaOH溶液时,减少的气体是二氧化硫和三氧化硫,所以三氧化硫和未参加反应的二氧化硫的体积是21.28L,剩余氧气的体积是5.6L,则参加反应的氧气的体积=0.7mol×22.4L/mol-5.6L=10.08L,根据二氧化硫、三氧化硫和氧气的关系式知,参加氧化还原反应的二氧化硫的体积=10.08L×2=20.16L,生成三氧化硫的体积=10.08L×2=20.16L,则未参加氧化还原反应的二氧化硫的体积=21.28L-20.16L=1.12L,原来二氧化硫的体积=20.16L+1.12L=21.28L,所以二氧化硫的转化率=$\frac{20.16L}{21.28L}$×100%=94.7%,
故答案为:94.7%;
(4)依据(3)的计算可知混合气体中生成三氧化硫气体物质的量=$\frac{20.16L}{22.4L/mol}$=0.9mol,在给定的条件下,溶液呈强酸性,BaSO3不会沉淀.
因此BaSO4的质量=0.9mol×5%×233g/mol=10.5g,
故答案为:10.5gBaSO4.
点评 本题考查平衡状态的判断、影响化学平衡的因素等知识点,对于反应前后气体的计量数之和不相等的可逆反应来说,可从浓度、温度、颜色、压强、百分含量等角度判断是否达到平衡状态,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 冰毒、黄连素 | B. | 海洛因、麻黄碱 | C. | 大麻、摇头丸 | D. | 黄曲霉素、尼古丁 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 如图所示①②③④分别是几种常见漏斗的上部,A、B、C、D是实际操作应用时,各漏斗的下部插入容器中的示意图.请指出A、B、C、D分别与①②③④相匹配的可能组合:A与③; B与②④(或①②④);C与①; D与④.
如图所示①②③④分别是几种常见漏斗的上部,A、B、C、D是实际操作应用时,各漏斗的下部插入容器中的示意图.请指出A、B、C、D分别与①②③④相匹配的可能组合:A与③; B与②④(或①②④);C与①; D与④.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
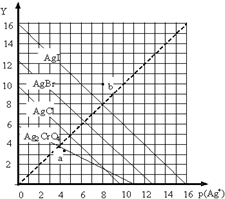 一定温度下,卤化银AgX(X:Cl-、Br-、I-)及Ag2CrO4的沉淀溶解平衡曲线如图示.横坐标p(Ag+)表示“-lgc(Ag+)”,纵坐标Y表示“-lgc(X-)”或“-lgc(CrO42-)”.下列说法正确的是( )
一定温度下,卤化银AgX(X:Cl-、Br-、I-)及Ag2CrO4的沉淀溶解平衡曲线如图示.横坐标p(Ag+)表示“-lgc(Ag+)”,纵坐标Y表示“-lgc(X-)”或“-lgc(CrO42-)”.下列说法正确的是( )| A. | a点表示c(Ag+)=c(CrO42-) | |
| B. | b点可表示AgI的饱和溶液 | |
| C. | 该温度下AgI的Ksp约为1×10-16 | |
| D. | 该温度下AgCl、AgBr饱和溶液中:c(Cl-)<c(Br-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 42g NaHCO3晶体中含有CO32-的数目为0.5NA | |
| B. | 1 mol OH-和17 g NH3所含的电子数相等 | |
| C. | 1 mol Cl2参加反应转移电子数一定为2NA | |
| D. | 2.0g H216O与D216O的混合物中所含中子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 为测定氯水的pH,用滴管吸取液体滴在pH试纸上,与标准比色卡对照即可 | |
| B. | 验证烧碱溶液中是否含有Cl-,先加稀硝酸除去OH-,再加入AgNO3溶液,有白色沉淀,证明含Cl- | |
| C. | 在未知溶液中滴加BaCl2溶液出现白色沉淀,加稀硝酸,沉淀不溶解,说明该未知溶液中存在SO42-或SO32- | |
| D. | 提纯混有少量硝酸钾的氯化钠,应采用在较高温度下制得浓溶液再冷却结晶、过滤、干燥的方法 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com