
����Ŀ����4mol A�����2mol B������2L���ܱ������ڻ�ϣ�����һ�������·������·�Ӧ��2A(g)+B(g)![]() 2C(g)������2s����C��Ũ��Ϊ0.6mol��L-1���������м���˵����
2C(g)������2s����C��Ũ��Ϊ0.6mol��L-1���������м���˵����
��������A��ʾ�ķ�Ӧ��ƽ������Ϊ0.3mol��L-1��s-1
��������B��ʾ�ķ�Ӧ��ƽ������Ϊ0.6mol��L-1��s-1
��2sʱ����A��ת����Ϊ70%
��2sʱ����B��Ũ��Ϊ0.7mol��L-1
������ȷ����
A���٢� B���٢� C���ڢ� ��D���ۢ�
���𰸡�B
��������
������������ݻ�ѧ��Ӧ���ʵ��ڵ�λʱ����Ũ�ȵı仯�������ݷ�Ӧ2A��g����B��g��![]() 2C��g��������������ʽ��������
2C��g��������������ʽ��������
��ʼA��Ũ��Ϊ4mol��2L��2mol/L
B��Ũ��Ϊ2mol��2L��1mol/L
2A��g��+B��g��![]() 2C��g��
2C��g��
��ʼŨ�ȣ�mol/L�� 2 1 0
ת��Ũ�ȣ�mol/L�� 0.6 0.3 0.6
2sʱŨ�ȣ�mol/L�� 1.4 0.7 0.6
��2s�ڣ�������A��ʾ�ķ�Ӧ��ƽ������Ϊv��A����0.6mol/L��2s��0.3molL-1s-1��
2s�ڣ�������B��ʾ�ķ�Ӧ��ƽ������Ϊv��B����0.3mol/L��2s��0.15molL-1s-1��
2sʱ����A��ת����Ϊ����![]()
2sʱ����B��Ũ��Ϊ0.7molL-1����Ȼ�٢���ȷ�����Դ�ѡB��


 ȫ��������ϵ�д�
ȫ��������ϵ�д� һ��һ����ʱ���ϵ�д�
һ��һ����ʱ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ������ͻ���������أ������й�˵���д�����ǣ� ��
A. ʳƷ��װ�г����й轺�������������
B. �ù�ҵ�ƾ��������þƳ������������
C. ������ˮʱ�����˻�ѧ�������仯������ˮ���ã���û��ɱ������������
D. ���д����Ͼɵ�أ��Է�ֹ��Ⱦ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ�Ƿ�������ʱ���õ������������ң����Խ��еĻ��������ֱ���
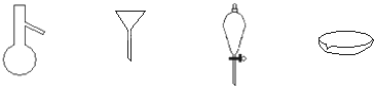
A��������������ȡ������
B�������ˡ���ȡ������
C����ȡ�����ˡ���������
D�����ˡ���������ȡ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����0.1mol/L��NaHCO3��Һ�������й�ϵʽ��ȷ������������
A. c(Na+)��c(HCO3-)��c(H+)��c(OH-) B. c(Na+)=c(HCO3-)��c(OH-)��c(H+)
C. c(Na+)+c(H+)��c(HCO3-)+c(OH-)+2c(CO32-) D. c(Na+)��c(HCO3-)+2c(CO32-)+c(H2CO3)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������ȷ���ǣ� ��
A. �Ȼ����л����������ʵ����ʣ����������ķ����ᴿ
B. ��ʹ��ʪ�ĵ���KI��ֽ�����ɫ������һ����Cl2
C. SO2��ʹ���Ը��������Һ��ɫ��������SO2��Ư����
D. Ũ���������ˮ�ԣ�������������������������NH3�ĸ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪����ʱ��0.1 molL��1 ijһԪ��HA ��ˮ����0.1%�������룬���������������
A������Һ�� pH��4
B�������¶ȣ���Һ��pH����
C������ĵ���ƽ�ⳣ��ԼΪ 1��10��7
D���� HA ������� c(H��)ԼΪˮ������� c(H��)��106��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪X��YԪ��ͬ���ڣ��ҵ縺��X>Y������˵���������
A. X��Y�γɻ�����ʱ��X�����Ը��ۣ�Y������
B. ��һ������Yһ��С��X
C. ��ۺ����������X������Y��
D. ��̬�⻯����ȶ���HbYС��HaX
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������£�����������Cl2��Ӧ��������HCl����
A. ���� B. ��ϩ C. �� D. ˮ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com