
| ||
| ||


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 已知R-CH═CH2+HX
已知R-CH═CH2+HX| Au |
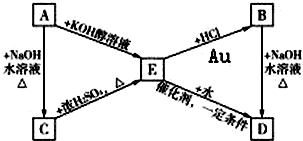
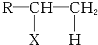 .如图中的A、B分别是分子式为C3H7Cl的两种同分异构体,请根据图中所示物质转化关系和反应条件,判断并写出:
.如图中的A、B分别是分子式为C3H7Cl的两种同分异构体,请根据图中所示物质转化关系和反应条件,判断并写出:查看答案和解析>>
科目:高中化学 来源: 题型:
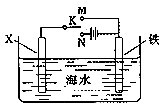
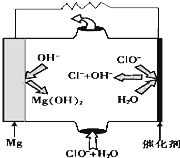 完成下列热化学方程式(化学方程式、电极反应式、表达式等)的书写:
完成下列热化学方程式(化学方程式、电极反应式、表达式等)的书写:| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| X | Y | ||
| W | Z | ||
| T |
| A、T元素的单质具有半导体的特性,T与Z元素可形成化合物TZ4 |
| B、X、Y、Z三种元素最低价氢化物的沸点依次升高 |
| C、由X、Y和氢三种元素形成的化合物中只有共价键 |
| D、物质WY2、W3X4、WZ4均有熔点高、硬度大的特性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、放电时,电子从正极流向电源的负极 | |||
| B、放电时,Li+向负极移动 | |||
C、该电池的总反应为LiNiO2+6C
| |||
| D、充电时,阳极发生的电极反应为Li1-xNiO2+xLi++x e-═LiNiO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| A、在Cu2O、Cu2S中Cu元素化合价都是+1价 |
| B、反应中Cu元素被氧化,S元素被还原 |
| C、Cu2S在反应中既是氧化剂,又是还原剂 |
| D、每生成6.4gCu,反应中转移0.1mol电子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com