
| A. | 100 mL 0.3 mol/L 的HCl 和50 mL 0.3 mol/L 的NaOH相混合 | |
| B. | 80mL 0.3 mol/L 的HCl 和80 mL 0.3 mol/L 的NaOH溶液相混合 | |
| C. | 80mL 0.3 mol/L 的H2SO4 和80 mL 0.3 mol/L 的NaOH溶液相混合 | |
| D. | 50mL 0.3 mol/L 的H2SO4 和50 mL 0.6 mol/L 的NaOH溶液相混合 |
分析 中和反应生成水的物质的量的越多,则放出的热量越多,注意计算各物质的物质的量,计算生成水的物质的量,进而比较放出的热量的多少即可.
解答 解:A.n(HCl)=0.03mol,n(NaOH)=0.015mol,则生成水0.015mol;
B.n(HCl)=0.024mol,n(NaOH)=0.024mol,则生成水0.024mol;
C.n(H2SO4)=0.024mol,n(NaOH)=0.024mol,则生成水0.024mol;
D.n(H2SO4)=0.015mol,n(NaOH)=0.03mol,则生成水0.03mol;
则D生成的水最多,放出的热量最多,
故选D.
点评 本题考查物质的量的计算,题目难度不大,注意判断反应的过量问题.


科目:高中化学 来源: 题型:选择题
| A. | $\frac{m(M-n)}{M}$ | B. | $\frac{M-n+2}{Mm}$ | C. | $\frac{m(M-n+2)}{M}$ | D. | $\frac{m(M-n-2)}{M}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 利用CO和H2合成甲醇,其反应的化学方程式为CO(g)+2H2(g)?CH3OH(g).今在一容积可变的密闭容器中,充有10mol CO和20mol H2用于合成甲醇.CO的平衡转化率(α)与温度(T)、压强(P)的关系如图所示:
利用CO和H2合成甲醇,其反应的化学方程式为CO(g)+2H2(g)?CH3OH(g).今在一容积可变的密闭容器中,充有10mol CO和20mol H2用于合成甲醇.CO的平衡转化率(α)与温度(T)、压强(P)的关系如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{78}^{202}$ Pt和${\;}_{78}^{198}$Pt的中子数相同,互称为同位素 | |
| B. | ${\;}_{78}^{202}$ Pt和${\;}_{78}^{198}$Pt的质子数相同,互称为同位素 | |
| C. | ${\;}_{78}^{202}$ Pt和${\;}_{78}^{198}$Pt不能互称为同位素 | |
| D. | ${\;}_{78}^{202}$Pt和${\;}_{78}^{198}$Pt是同一种核素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 33% | B. | 40% | C. | 50% | D. | 67% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaCl MgCl2 Na2O | B. | H2O Na2O CO2 | ||
| C. | CaCl2 NaOH H2SO4 | D. | NH4Cl H2O CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4种 | B. | 3种 | C. | 2种 | D. | 1种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素代号 | A | B | F |
| 原子半径/nm | 0.077 | 0.075 | 0.117 |
| 主要化合价 | +4、-4 | +5、-3 | +4、-4 |
| 元素 | D | M | G | E |
| 性质 结构 信息 | 单质制成的高压灯,发出的黄光透雾力强、射程远. | 氢化物常温下呈液态,M的双原子阴离子有18个电子 | 原子核外的M层比L层少2个电子. | +3价阳离子的核外电子排布与氖原子相同. |
 ,钙与A原子个数比为1:2化合物含有的化学键类型(填离子键、共价键或非极性键)离子键和非极性键共价键.
,钙与A原子个数比为1:2化合物含有的化学键类型(填离子键、共价键或非极性键)离子键和非极性键共价键.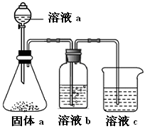
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com