
(8分)如图,曲线表示在 时,和某反应有关的物质A、B、C的物质的量浓度从开始反应至4分钟时的变化图像,试回答:
时,和某反应有关的物质A、B、C的物质的量浓度从开始反应至4分钟时的变化图像,试回答:

(1)该反的反应物是 。
(2)4分钟时,C的浓度是B的 倍。
(3)该反应的化学方程式是
(4)反应开始至4分钟,若用A的浓度来表示该反应的平均速率为
科目:高中化学 来源: 题型:阅读理解

| 实验现象 | 原因 |
| 溶液最初从紫色逐渐变为 红 红 色 |
氯气与水反应生成的酸电离出的H+使石蕊变色 氯气与水反应生成的酸电离出的H+使石蕊变色 |
| 随后溶液逐渐变为无色 | 氯气与水反应生成的次氯酸具有强氧化性将其漂白褪色 氯气与水反应生成的次氯酸具有强氧化性将其漂白褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解


| 实验现象 | 原因 |
| 溶液最初从紫色逐渐变为 红 红 色 |
氯气与水反应生成的H+使石蕊变色 |
| 随后溶液逐渐变为无色 | 氯气与水反应生成的HClO将石蕊氧化为无色物质 氯气与水反应生成的HClO将石蕊氧化为无色物质 |
| 然后溶液从无色逐渐变为 黄绿 黄绿 色 |
继续通入的氯气溶于水使溶液呈黄绿色 继续通入的氯气溶于水使溶液呈黄绿色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
(8分)室温下,将1.00mol/L盐酸滴入20.00mL 1.00mol/L氨水中,溶液pH和温度(0C)
随加入盐酸体积变化曲线如右图所示。
(1)下列有关说法正确的是___________
A.a点由水电离出的C(H+)=10-14mol/L
B.b点:
C.c点:C(Cl-)=C(NH4+)
D.d点后,容易温度略下降的主要原因是NH3·H2O电离吸热
(2)在滴加过程中,水的电离程度的变化是先 后 (填“增大”、“减小”或“不变”);
(3)在下表中,分别讨论了上述实验过程中离子浓度的大小顺序,对应溶质的化学式和
溶液的pH。试填写表中空白:
|
| 离子浓度的关系 | 溶质 | 溶液的pH | 物料守恒关系 |
| ① | C(NH4+)>C(Cl-)>C(OH-)>C(H+) |
| pH>7 | / |
| ② |
| NH4Cl | / |
|
| ③ | C(Cl-)>C(H+)>C(NH4+)>C(OH-) |
| pH<7 | / |
查看答案和解析>>
科目:高中化学 来源: 题型:
(14分)磷酸(H3PO4)在水中可分三步电离,能够以H3PO4、H2PO- 4、HPO2- 4、PO3- 4等四种粒子形式存在,当溶液的pH发生变化时,其中任一粒子的物质的量占四种粒子总物质的量的分数δ(分布分数)也可能发生变化。图1是某浓度H3PO4溶液中各种粒子的物质的量分数δ随pH的变化曲线。用NaOH标准溶液滴定该H3PO4溶液,绘得滴定曲线如图2。
图1 H3PO4粒子分部分数与pH关系 图2 H3PO4滴定曲线(部分)
(注:图中曲线1表示H3PO4、曲线2表示H2PO- 4、曲线3表示HPO2- 4、曲线4表示PO3- 4)
(1)H3PO4第一步电离的电离常数K1的表达式为_______,K1的数值最接近(填字母)______。
A.10-2.1 B.10-4.7 C.10-7 D.10-9.7
(2)用NaOH滴定H3PO4,写出反应从a点到b点的离子方程式____________________,当滴定至pH=7时,溶液主要存在的阴离子(OH-除外)有_______________。
(3)在Na3PO4溶液中,![]() ____3(填“>”、“<”、“=”),原因是__________________(用离子方程式表示)。
____3(填“>”、“<”、“=”),原因是__________________(用离子方程式表示)。
(4)磷酸钙、磷酸一氢钙和磷酸二氢钙是三种重要的磷酸盐,在食品、化肥等方面应用广泛。其20℃时溶解度数据如下表:
| 名称 | 化学式 | 20℃时溶解度(g) |
| 磷酸钙 | Ca3(PO4)2 | 2×10-3 |
| 磷酸一氢钙 | CaHPO4 | 4.3×10-3 |
| 磷酸二氢钙 | Ca(H2PO4)2 | 1.8 |
磷酸钙在水中溶解度很小,但易溶于稀盐酸。结合平衡移动原理分析其原因
_________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年高考化学一轮复习《化学反应速率与化学平衡》专题综合测试(苏教版) 题型:填空题
(8分)在2 L密闭容器内,800℃时反应2NO(g)+O2(g)  2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
|
时间/s |
0 |
1 |
2 |
3 |
4 |
5 |
|
n(NO)/mol |
0.020 |
0.010 |
0.008 |
0.007 |
0.007 |
0.007 |
(1)写出该反应的平衡常数表达式:K=________。
已知:K300℃>K350℃,则该反应是________热反应。
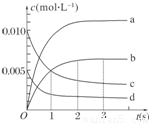
(2)如图中表示NO2的变化的曲线是________。用O2表示从0~2 s内该反应的平均速率v=________________________________________________________________________。
(3)能说明该反应已达到平衡状态的是________。
a.v(NO2)=2v(O2)
b.容器内压强保持不变
c.v逆(NO)=2v正(O2)
d.容器内密度保持不变
(4)能使该反应的反应速率增大,且平衡向正反应方向移动的是________。
a.及时分离出NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com