
| Ԫ�� | �� �� �� Ϣ |
| A | Ԫ����Ҫ���ϼ�Ϊ-2��ԭ�Ӱ뾶Ϊ0.074nm |
| B | ��������������������������֮��Ϊ4 |
| C | ԭ�Ӱ뾶Ϊ0.102nm���䵥��Ϊ��ɫ���壬����A�ĵ�����ȼ�� |
| D | ����������ˮ�����ܰ�1��1�������������ȵ����������� |
| E | ԭ�Ӱ뾶Ϊ0.075nm������������ˮ����������⻯���γ�һ����X |
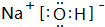 ��
��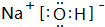 ��
��| 80g |
| 64g/mol |


 ������ϰ�ο����뵥Ԫ���ϵ�д�
������ϰ�ο����뵥Ԫ���ϵ�д� �����Ծ���ĩ���100��ϵ�д�
�����Ծ���ĩ���100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��62 g Na2O��Һ��ˮ��������Һ�к��е�O2-��ΪNA |
| B����״���£�6.72L NO2��ˮ��ַ�Ӧת�Ƶĵ�����ĿΪ0.1NA |
| C�����³�ѹ�£�16g���飨12C1H��������������Ϊ10NA |
| D�����³�ѹ�£�14g��N2��CO��ɵĻ�����庬�е�ԭ����ĿΪNA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
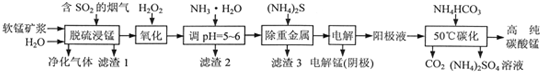
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| c(OH-) |
| c(H+) |
| A��0.01mol?L-1 HA����Һ��c��H+��=1��10-4mol?L-1 |
| B��pH=3��HA��Һ��pH=11��NaOH��Һ�������Ϻ�������Һ��c��Na+����c��A-����c��OH-����c��H+�� |
| C��pH=3��HA��Һ��pH=11��NaOH��Һ�������1��10��Ϻ�������Һ��c��OH-��+c��A-��=c��H+��+c��Na+�� |
| D��Ũ�Ⱦ�Ϊ0.1 mol?L-1��HA��Һ��NaA��Һ�������Ϻ�������Һ�����ԣ���c��OH-��-c��H+����c��HA��-c��A-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ǿ������γɵ���Һ�䵼������һ��ǿ |
| B��Ũ����ͬ��ǿ���������������γɵ���Һ��������ʵĵ����������� |
| C��BaSO4������ˮ����ˮ��Һ�ĵ�����������������Ϊ������� |
| D����������κ�״̬�¶��ܵ��� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com