
书写离子方程式(8分)
(1) 铜和足量浓硝酸反应的离子方程式为
(2)二氧化锰与足量浓盐酸反应的离子方程式为:
(3)向碳酸氢钾溶液中滴入少量澄清石灰水反应的离子方程式为:
(4)向明矾溶液中加入过量的氢氧化钡溶液反应的离子方程式为
【答案】21.书写离子方程式(8分)
(1) Cu+4H+ +2NO3-═Cu2++2H2O+NO2↑ (2)MnO2+4H++2Cl-=Mn2++Cl2↑+2H2O
(3)2HCO3-+Ca2++2OH-=CO32-+2H2O+CaCO3↓ (4)Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O
【解析】
试题分析:根据书写原则:单质、气体、氧化物、弱酸、弱碱、难溶盐写成化学式,强酸、强碱、可溶性的盐写成离子形式,(1)铜和足量浓硝酸反应,铜、水、气体写成化学式,其余拆开,可得:Cu+4H+ +2NO3-═Cu2++2H2O+NO2↑(2)二氧化锰与足量浓盐酸反应,氧化物、气体、水写成化学式,其余拆开,可得MnO2+4H++2Cl-=Mn2++Cl2↑+2H2O(3)依据“以少定多”的原则,向碳酸氢钾溶液中滴入少量澄清石灰水反应的离子方程式为:2HCO3-+Ca2++2OH-=CO32-+2H2O+CaCO3↓(4)依据“以少定多”的原则,向明矾溶液中加入过量的氢氧化钡溶液反应的离子方程式为:Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O
考点:考查离子方程式的书写。


科目:高中化学 来源: 题型:
按下图所示的装置进行实验:
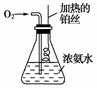
(1)实验开始一段时间后,可观察到锥形瓶瓶口上方有白烟生成,请补充可能观察到的其他现象:______________________________________________;
有关化学方程式为__________________________________________________。
(2)由于气温的原因,上述实验一段时间后现象不太明显,需要向锥形瓶内加入下列哪种物质才能重新看到明显的现象?________。
A.NaOH B.CaO
C.浓H2SO4 D.NH4Cl
(3)经过对比实验证明,在其他条件相同时,用空气代替氧气的实验效果较差,主要原因是________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下0.1mol·L-1醋酸溶液的pH=a,下列能使溶液pH=(a+1)的措施是
A.将溶液稀释到原体积的10倍 B.加入适量的醋酸钠固体
C.加入等体积0.2 mol·L-1盐酸 D.提高溶液的温度
查看答案和解析>>
科目:高中化学 来源: 题型:
已知 蒸发1mol Br2(l)需要吸收的能量为30kJ,其它相关数据如下表:
蒸发1mol Br2(l)需要吸收的能量为30kJ,其它相关数据如下表:
| H2(g) | Br2(g) | HBr(g) | |
| 1mol分子中的化学键断裂时需要吸收的能量/kJ | 436 | a | 369 |
则表中a为
A.404 B.260 C.230 D.200
查看答案和解析>>
科目:高中化学 来源: 题型:
某学生用0.1000mol/LKOH溶液滴定未知浓度的盐酸溶液,其操作可分解为如
下几步
A 移取20.00mL待测的盐酸溶液注入洁净的锥形瓶,并加入2-3滴酚酞
B 用标准溶液润洗滴定管2-3次
C 把盛有标准溶液的碱式滴定管固定好,调节液面使滴定管尖嘴充满溶液
D.取标准KOH溶液注入碱式滴定管至0刻度以上2-3cm
E.调节液面至0或0刻度以下,记下读数
F.把锥形瓶放在滴定管的下面,用标准KOH溶液滴定至终点,记下滴定管液面刻度
(1) 正确操作的顺序是(用序号字母填写) B- 。
(2) 滴定开始后,眼睛注视 ,判断滴定终点的现象是:
(3) 下列操作中可能使所测盐酸的浓度数值偏高的是
A 碱式滴定管未用标准溶液润洗就直接注入标准液
B 滴定前盛放HCl的锥形瓶用蒸馏水洗净后有少量水残留
C 碱式滴定管在滴定前有气泡,滴定后气泡消失
D 读取氢氧化钠溶液时,开始仰视读数,滴定结束时俯视读数
(4)滴定开始和结束时,碱式滴定管中的液面如图C所示,则终点读数为 mL,所测盐酸溶液的浓度为 mol/L。

查看答案和解析>>
科目:高中化学 来源: 题型:
红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)。反应过程和能量关系如图所示:

(图中的ΔH表示生成1 mol产物的数据)。
(1)P和Cl2反应生成PCl3的热化学方程式是____________________________。
(2)PCl5分解成PCl3和Cl2的热化学方程式是__________ _______________。
_______________。
(3)P和Cl2分两步反应生成1 mol PCl5的ΔH3=__________,P和Cl2一步反应生成1 mol PCl5的ΔH4_ ______________ΔH3 (填“大于”“小于”或“等于”)。
______________ΔH3 (填“大于”“小于”或“等于”)。
(4)PCl5与足量水充分反应,最终生成两种酸,其化学方程式是______________。
(1)(2)反应物和反应产物互换时,ΔH数值不变,注意变号。
(3)总反应的焓变,可以看做是各步反应焓变的加和。
(4)PCl5与水反应时,化合价未发生变化,可依此分析出酸为磷酸和盐酸。
查看答案和解析>>
科目:高中化学 来源: 题型:
铁、铝、铜及其化合物在生产、生活中有广泛的用途,试回答下列问题:
(1)铁、铝、铜三种金属的金属活动性由弱到强的排列顺序是__________。
(2)制造电路板的工艺中,FeCl3溶液可以蚀刻铜箔,请写出该反应的离子方程式:__ ___。
(3)已知铜与稀硫酸不反应,但铜片在稀硫酸中长时间加热时溶液会呈蓝色,请用化学方程式表示其原因: _________________________________________。
(4)氯化铝广泛用作有机合成和石油工业的催化剂。将铝土矿粉(主要成分为A12 03)与焦炭混合后加热并通人氯气,可得到氯化铝,同时生成CO,写出该反应的化学方程式:________________________ ,该反应的氧化剂是_________________。
(5)某校兴趣小组为测定一种铁铝硅合金 (FexAlySiz) 粉末的组成,提出如下方案:准确称取1.46 g该合金粉末,加入过量盐酸溶液,充分反应后过滤,测定剩余固体质量0.07 g。向滤液中滴加足量NaOH浓溶液,充分搅拌、过滤、洗涤得固体。再将所得固体充分加热、灼烧,得红棕色粉末1.60g,通过计算确定此合金的组成为________________ (填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
向100 mL 0.25 mol·L-1 AlCl3溶液中加入金属钠,使之溶解,恰好生成只含有NaCl和Na[Al(OH)4]的澄清溶液,则加入的金属钠的质量是( )
A.3.45 g B.2.3 g
C.1.15 g D.0.575 g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com