
| A. | 只有②③ | B. | 只有③④ | C. | ①②③④ | D. | 只有①③④ |
分析 结构相似,在分子组成上相差一个或若干个CH2原子团的物质互称为同系物.同系物具有如下特点:结构相似、化学性质相似、分子式通式相同,分子式不同、物理性质不同,研究范围是有机物,同分异构体的物理性质和化学性质可能都不同,据此分析.
解答 解:①同系物结构相似,化学性质相似,但化学性质相似物质不一定是同系物,如乙醇与甘油,故错误;
②只有结构相似时,分子组成相差一个或几个CH2原子团的有机物才是同系物,故错误;
③烃中碳、氢元素的质量分数相同,可能是同系物也可能是同分异构体,还可能是最简式相同的物质,故错误;
④具有相同C原子数的醇与醚,酸与酯等,物理性质和化学性质都不相同,故错误;
故选C.
点评 本题考查同系物、同分异构体等,难度中等,解题关键是同系物的概念,掌握同系物的相关知识是解题关键.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3Br | B. | CH3CH2CH2CH2Br | C. | CH2BrCH2Br | D. | CH3CHBrCH2CH2Br |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2和CO2 | B. | CO2和H2O | C. | CO和CH3OH | D. | CH3OH和H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 基态原子是处于最低能量状态的原子 | |
| B. | 基态C原子的电子排布式是1s22s12p3 | |
| C. | 焰色反应是金属原子的电子从基态跃迁到激发态时产生的光谱 | |
| D. | 同一原子处于激发态时的能量一定低于基态时的能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
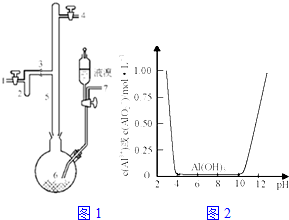 利用废铝箔(主要成分为Al、少量的Fe、Si等)既可制取有机合成催化剂AlBr3又可制取净水剂硫酸铝晶体.
利用废铝箔(主要成分为Al、少量的Fe、Si等)既可制取有机合成催化剂AlBr3又可制取净水剂硫酸铝晶体.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com