
下列说法正确的是( )
A.1L水中溶解了58.5gNaCl,该溶液的物质的量浓度为1mol/L
B.从1L 2mol/L的H2SO4溶液中取出0.5L,该溶液的浓度为1mol/L
C.配制500mL 0.1mol/L的CuSO4溶液,需8.0g硫酸铜固体
D.0.1mol/L MgCl2溶液中Cl-浓度为0.1mol/L
科目:高中化学 来源:2017届浙江省高三上统考四化学试卷(解析版) 题型:选择题
下列有关实验能成功的是
A.苯加到溴水中,将会和溴发生取代反应而使溴水褪色
B.用冷却结晶法来提纯含少量KCl杂质的KNO3晶体
C.将10%的葡萄糖溶液加到新制氢氧化铜悬浊液中,出现砖红色沉淀
D.进行淀粉水解实验时 ,为检验水解产物和水解程度,加液顺序为:淀粉溶液→H2SO4溶液→NaOH溶液→碘水→新制Cu(OH)2悬
,为检验水解产物和水解程度,加液顺序为:淀粉溶液→H2SO4溶液→NaOH溶液→碘水→新制Cu(OH)2悬 浊液
浊液
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高一上学期月考二化学试卷 (解析版) 题型:选择题
下列变化需要加入适当的氧化剂才能完成的是( )
A.CuO→Cu B.Fe→FeCl2 C.H2SO4→H2 D.HNO3→N2
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省等三校高一上联考二化学卷(教师版) 题型:填空题
(1)已知物质由H、C、Na、O、Cl、Fe元素中的一种或几种组成。请按要求回答。
①酸性氧化物的化学式 。(写一种,下同)
②有机物的化学式 。
③碱性氧化物与酸反应的离子方程式 。
(2)依据题意填空。
①填入合适的符号。 + 2H+ = CO2↑+ H2O + Ba2+
②写出离子方程式为Cu2+ + 2OH- =Cu(OH)2↓的化学方程式。 (写一个)
③用氯化铁溶液腐蚀铜线路板的离子方程式为________________。
④将氯气通入NaOH 溶液中可生产消毒液。写出发生反应的离子方程式______________,并用单线桥或双线桥标出电子转移的方向和数目。_____________________
(3)选择合适的试剂除去下列括号内的杂质。
选择的试剂 | 操作 | 选择的试剂 | |
①Cu(Fe) | ②CO2气体(HCl) |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省协作校高二上学期期中化学卷(解析版) 题型:实验题
工业废水中常含有一定量的Cr2O72-和CrO42-,它们会对人类及生态系统产生很大的伤害,必须进行处理。常用的处理方法是还原沉淀法。该法的工艺流程为: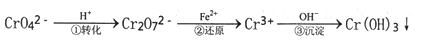
其中第①步存在平衡:2 CrO42-(黄色)+2H+ Cr2O72- (橙色)+H2O
Cr2O72- (橙色)+H2O
(1) 若平衡体系的pH=12,则溶液显_______色。
(2) 能说明第①步反应达平衡状态的是______________。
a.Cr2O72-和CrO42-的浓度不变
B.2v(Cr2O72-) =v(CrO42-)
C.溶液的颜色不变
(3)第②步中,还原lmol Cr2O72-离子,需要_______mol的FeSO4•7H2O。
(4)第③步生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:
Cr (OH)3 (s) Cr3+ (aq) +3OH- (aq)
Cr3+ (aq) +3OH- (aq)
常温下,Cr(OH)3的溶度积Ksp=c(Cr3+)·c3(OH-) = 10-32,要使0.01mol/Lc(Cr3+)开始沉淀,溶液的pH应调至__________,若使c(Cr3+)降至10-5mol/L,溶液的pH应调至___________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省协作校高二上学期期中化学卷(解析版) 题型:选择题
某炔烃含有一个三键,与H2发生加成后的产物为: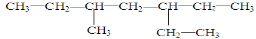 则该炔烃可能具有的结构有
则该炔烃可能具有的结构有
A.1种 B.2种 C.3种 D.4种
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省沈阳市城郊市重点联合体高一上期中化学卷(解析版) 题型:实验题
用质量分数98%、密度为1.84g·cm-3的浓硫酸配制480mL0.92mol·L-1的稀硫酸
(1)配制时,除量筒、烧杯、玻璃棒外还需玻璃仪器有 、 、 。
(2)减小误差量取时需选用合适的量筒量取 mL浓硫酸
(3)在容量瓶的使用方法中,下列操作不正确的是________。
A.使用容量瓶前检查它是否漏水 |
B.容量瓶用蒸馏水洗净后,再用待配溶液润洗 |
C.配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,缓慢加入蒸馏水到接近标线1~2cm处,改用胶头滴管加蒸馏水到标线 |
D.往容量瓶中转移溶液时应用玻璃棒引流 |
(4)在配制过程中,其他操作都是正确的,下列操作会引起误差偏高的是__________。
①转移溶液时不慎有少量洒到容量瓶外面 ②没有洗涤烧杯和玻璃棒③定容时俯视刻度线④容量瓶不干燥,含有少量蒸馏水⑤定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线。⑥未冷却到室温就将溶液转移到容量瓶并定容
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高二上学期期中化学试卷(解析版) 题型:填空题
(1)目前国际空间站处理CO2的一个重要方法是将CO2还原,所涉及的反应方程式为:CO2(g)+4H2(g)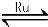 CH4(g)+2H2O(g) △H﹤0
CH4(g)+2H2O(g) △H﹤0
则升高温度平衡体系中H2的体积分数将___________;(选填“增大”、“减小”或“不变”)
(2)相同温度时,上述反应在不同起始浓度下分别达到平衡,各物质的平衡浓度如下表:
[CO2]/mol·L-1 | [H2]/mol·L-1 | [CH4]/mol·L-1 | [H2O]/mol·L-1 | |
平衡Ⅰ | a | b | c | d |
平衡Ⅱ | m | n | x | y |
a、b、c、d与m、n、x、y之间的关系式为_________。
(3)人体血液中的碳酸和碳酸氢盐存在平衡:H++ HCO3- H2CO3,当有少量酸性或碱性物质进入血液中时,血液的pH变化不大,用平衡移动原理解释上述现象。____________________
H2CO3,当有少量酸性或碱性物质进入血液中时,血液的pH变化不大,用平衡移动原理解释上述现象。____________________
(4)查阅资料获知如下信息:
i.H2CO3:Ki1=4.3×10-7,Ki2=5.6×10-11(以Ki1为主)
ii.标况下,CO2的溶解度为约为1:1
iii.H2O+CO2  H2CO3
H2CO3 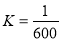
iv. 

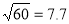 ㏒(6)=0.8
㏒(6)=0.8
请尝试估算:
①饱和二氧化碳溶液中碳酸的物质的量浓度c(H2CO3)约为_______________mol/L;
②饱和二氧化碳溶液中碳酸的电离度α约为_____________。
③正常雨水的pH约为____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com