
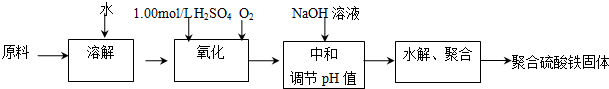
·ÖĪö £Ø1£©¢ŁÅäÖĘŅ»¶ØĪļÖŹµÄŹĒÅØ¶ČµÄČÜŅŗŅŖ³ĘĮæČÜÖŹµÄÖŹĮ棬ÓĆČŻĮæĘæ¶ØČŻ£»
¢ŚĮņĖįŃĒĢśŌŚĖįŠŌĢõ¼žĻĀ±»ŃõĘųŃõ»Æ³ÉĮņĖįĢś£»
£Ø2£©ĮņĖį¹ż¶ą£¬ŌŚŗóĆęµ÷½ŚpHŹ±ŅŖĻūŗĵÄĒāŃõ»ÆÄʵÄĮæ¾Ķ¶ą£¬Ōģ³ÉĄĖ·Ń£»
£Ø3£©¢Ł²ÉÓĆÖŲĮæ·Ø²ā¶Ø¼īŹ½ĮņĖįĢś£Øx Fe2O3•y SO3•z H2O£©ÖŠx”¢y”¢zµÄÖµŹ±£¬æÉŅŌ½«ŃłĘ·ČÜÓŚĒāŃõ»ÆÄĘČÜŅŗ£¬øł¾ŻµĆµ½µÄ¹ĢĢåŃõ»ÆĢśµÄÖŹĮæČ·¶ØxµÄÖµ£¬¹żĀĖ£¬ŌŚĖłµĆĀĖŅŗÖŠ¼ÓĀČ»Æ±µ£¬øł¾Ż²śÉśµÄĮņĖį±µ³ĮµķµÄÖŹĮææÉČ·¶ØyµÄÖµ£¬øł¾ŻŃłĘ·µÄ×ÜÖŹĮæ½įŗĻFe2O3ŗĶ¼ĘĖćµĆµÄSO3µÄÖŹĮææÉČ·¶ØzµÄÖµ£»
¢Śøł¾Ż¢ŁµÄ·ÖĪöæÉÖŖ£¬ŅŖ²ā¶ØFe2O3”¢BaSO4µÄÖŹĮ棻
£Ø4£©²ā¶Ø¹ż³ĢÖŠ½«ŃłĘ·ČÜÓŚĒāŃõ»ÆÄĘČÜŅŗ£¬¾¹ż¹żĀĖ”¢Ļ“µÓ”¢ŗęøÉ»ņ×ĘÉÕ”¢ĄäČ“”¢³ĘĮæµĆŃõ»ÆĢśµÄÖŹĮ棬ŌŚĖłµĆĀĖŅŗÖŠ¼ÓĀČ»Æ±µ£¬¾¹ż¹żĀĖ”¢Ļ“µÓ”¢ŗęøÉ»ņ×ĘÉÕ”¢ĄäČ“”¢³ĘĮæµĆĮņĖį±µµÄÖŹĮ棬¾Ż“Ė“šĢā£®
½ā“š ½ā£ŗ£Ø1£©¢ŁÅäÖĘŅ»¶ØĪļÖŹµÄŹĒÅØ¶ČµÄČÜŅŗŅŖ³ĘĮæČÜÖŹµÄÖŹĮ棬ŅŖÓƵē×ÓĢģĘ½£¬ÓĆČŻĮæĘæ¶ØČŻ£¬
¹Ź“š°øĪŖ£ŗµē×ÓĢģĘ½”¢ČŻĮæĘ棻
¢ŚĮņĖįŃĒĢśŌŚĖįŠŌĢõ¼žĻĀ±»ŃõĘųŃõ»Æ³ÉĮņĖįĢś£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ4Fe2++O2+4H+4Fe3++2H2O£¬
¹Ź“š°øĪŖ£ŗ4Fe2++O2+4H+4Fe3++2H2O£»
£Ø2£©ĮņĖįÉŌ¹żĮæŹĒĪŖĮĖ·ĄÖ¹Fe3+Ė®½ā³ÉĒāŃõ»ÆĢś£¬µ±ĮņĖį¹ż¶ąŹ±£¬ŗóŠųÖŠŗĶŠčŅŖµÄ¼īµÄÓĆĮæĮ¦“ó£¬Ōģ³ÉĄĖ·Ń£¬ĖłŅŌ¼ÓČėµÄĮņĖį±ČĄķĀŪÖµÉŌ¶ą£¬µ«²»Äܹż¶ą£¬
¹Ź“š°øĪŖ£ŗĮņĖįÉŌ¹żĮæŹĒĪŖĮĖ·ĄÖ¹Fe3+Ė®½ā³ÉĒāŃõ»ÆĢś£¬µ±ĮņĖį¹ż¶ąŹ±£¬ŗóŠųÖŠŗĶŠčŅŖµÄ¼īµÄÓĆĮæĮ¦“ó£¬Ōģ³ÉĄĖ·Ń£»
£Ø3£©¢Ł²ÉÓĆÖŲĮæ·Ø²ā¶Ø¼īŹ½ĮņĖįĢś£Øx Fe2O3•y SO3•z H2O£©ÖŠx”¢y”¢zµÄÖµŹ±£¬æÉŅŌ½«ŃłĘ·ČÜÓŚĒāŃõ»ÆÄĘČÜŅŗ£¬øł¾ŻµĆµ½µÄ¹ĢĢåŃõ»ÆĢśµÄÖŹĮæČ·¶ØxµÄÖµ£¬¹żĀĖ£¬ŌŚĖłµĆĀĖŅŗÖŠ¼ÓĀČ»Æ±µ£¬øł¾Ż²śÉśµÄĮņĖį±µ³ĮµķµÄÖŹĮææÉČ·¶ØyµÄÖµ£¬øł¾ŻŃłĘ·µÄ×ÜÖŹĮæ½įŗĻFe2O3ŗĶ¼ĘĖćµĆµÄSO3µÄÖŹĮææÉČ·¶ØzµÄÖµ£¬¹ŹŃ”a c£»
¢Śøł¾Ż¢ŁµÄ·ÖĪöæÉÖŖ£¬ŅŖ²ā¶ØFe2O3”¢BaSO4µÄÖŹĮ棬
¹Ź“š°øĪŖ£ŗFe2O3”¢BaSO4£»
£Ø4£©²ā¶Ø¹ż³ĢÖŠ½«ŃłĘ·ČÜÓŚĒāŃõ»ÆÄĘČÜŅŗ£¬¾¹ż¹żĀĖ”¢Ļ“µÓ”¢ŗęøÉ»ņ×ĘÉÕ”¢ĄäČ“”¢³ĘĮæµĆŃõ»ÆĢśµÄÖŹĮ棬ŌŚĖłµĆĀĖŅŗÖŠ¼ÓĀČ»Æ±µ£¬¾¹ż¹żĀĖ”¢Ļ“µÓ”¢ŗęøÉ»ņ×ĘÉÕ”¢ĄäČ“”¢³ĘĮæµĆĮņĖį±µµÄÖŹĮ棬¹ŹŃ”aed£®
µćĘĄ ±¾Ģāæ¼²éĪļÖŹµÄ·ÖĄėŗĶĢį“棬²ąÖŲæ¼²éѧɜ»ńČ”ŠÅĻ¢¼°ĄūÓĆŠÅĻ¢ÄÜĮ¦”¢·ÖĪöÄÜĮ¦”¢ŹµŃé²Ł×÷ÄÜĮ¦£¬×¢ŅāĢāøųŠÅĻ¢µÄĮé»īŌĖÓĆ£¬ÖŖµĄ³£¼ūĄė×ӵļģŃé·½·Ø¼°ĻÖĻó£¬ĢāÄæÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ³£ĪĀ³£Ń¹ĻĀ£¬14gŅ»Ńõ»ÆĢ¼ĖłÕ¼Ģå»żĪŖ11.2 L | |
| B£® | µČĪļÖŹµÄĮæµÄNa2O2ŗĶNa2OÖŠĖłŗ¬ŅõŃōĄė×Ó×ÜŹżĻąµČ | |
| C£® | NOµÄĦ¶ūÖŹĮæĪŖ30g | |
| D£® | ³£ĪĀ³£Ń¹ĻĀ32g³ōŃõÖŠŗ¬ÓŠµÄŃõŌ×ÓŹżÄæ±Č±ź×¼×“æöĻĀ22.4LŃõĘųÖŠŗ¬ÓŠµÄŃõŌ×ÓŹżÄæÉŁ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
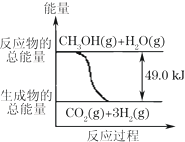 ¼×“¼ÖŹ×Ó½»»»Ä¤Č¼ĮĻµē³ŲÖŠ½«¼×“¼ÕōĘų×Ŗ»ÆĪŖĒāĘųµÄĮ½ÖÖ·“Ó¦ŌĄķŹĒ£ŗ
¼×“¼ÖŹ×Ó½»»»Ä¤Č¼ĮĻµē³ŲÖŠ½«¼×“¼ÕōĘų×Ŗ»ÆĪŖĒāĘųµÄĮ½ÖÖ·“Ó¦ŌĄķŹĒ£ŗ| A£® | 1molCH3OHĶźČ«Č¼ÉÕ·ÅČČ192.9kJ | |
| B£® | ·“Ó¦¢ŁÖŠµÄÄÜĮæ±ä»ÆČēÓŅĶ¼ĖłŹ¾ | |
| C£® | CH3OH×Ŗ±ä³ÉH2µÄ¹ż³ĢŅ»¶ØŅŖĪüŹÕÄÜĮæ | |
| D£® | øł¾Ż¢ŚĶĘÖŖ·“Ó¦£ŗCH3OH£Øl£©+$\frac{1}{2}$ O2£Øg£©”śCO2£Øg£©+2H2£Øg£©+QµÄQ£¼192.9kJ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ·ÅµēŹ±£¬øŗ¼«µÄµē¼«·“Ó¦Ź½£ŗLi-e-ØTLi+ | |
| B£® | ³äµēŹ±£¬Li0.85NiO2Ö»·¢ÉśŃõ»Æ·“Ó¦ | |
| C£® | øƵē³Ų²»ÄÜÓĆĖ®ČÜŅŗ×÷ĪŖµē½āÖŹ | |
| D£® | ·Åµē¹ż³ĢÖŠLi+ĻņÕż¼«ŅĘ¶Æ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ŃōĄė×Ó | K+ Na+ Cu2+ Al3+ |
| ŅõĄė×Ó | SO42- HCO3-OH- Cl- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŃĪĖįÓėNaOHČÜŅŗ·“Ó¦ | B£® | Ģ¼ĖįĒāļ§ŹÜČČ·Ö½ā | ||
| C£® | ĀĮ·ŪÓėMnO2·“Ó¦ | D£® | Ńõ»ÆøĘČÜÓŚĖ® |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com