
±±¾©°ĀŌĖ»į”°ĻéŌĘ”±»š¾ęČ¼ĮĻŹĒ±ūĶé(C3H8)£¬ŃĒĢŲĄ¼“ó°ĀŌĖ»į»š¾ęČ¼ĮĻŹĒ±ūĻ©(C3H6)£®
(1)±ūĶéĶŃĒāæɵƱūĻ©£®ŅŃÖŖ£ŗ
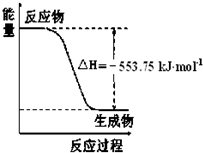
C3H8(g)ŌņĻąĶ¬Ģõ¼žĻĀ£¬·“Ó¦C3H8(g)![]() CH3CH£½CH2(g)£«H2(g)µÄ¦¤H£½________kJ”¤mol£1£®
CH3CH£½CH2(g)£«H2(g)µÄ¦¤H£½________kJ”¤mol£1£®
(2)ŅŌ±ūĶéĪŖČ¼ĮĻÖĘ×÷ŠĀŠĶČ¼ĮĻµē³Ų£¬µē³ŲµÄÕż¼«ĶØČėO2ŗĶCO2£¬øŗ¼«ĶØČė±ūĶ飬µē½āÖŹŹĒČŪČŚĢ¼ĖįŃĪ£®µē³Ų·“Ó¦·½³ĢŹ½ĪŖ________£»·ÅµēŹ±£¬CO32£ŅĘĻņµē³ŲµÄ________(Ģī”°Õż”±»ņ”°øŗ”±)¼«£®
 æŖŠÄĶÜדŌŖ²āŹŌ¾ķĻµĮŠ“š°ø
æŖŠÄĶÜדŌŖ²āŹŌ¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
 HCO3-+H+µÄĘ½ŗā³£ŹżK1=
HCO3-+H+µÄĘ½ŗā³£ŹżK1= CO32-+H+£¬HCO3-+H2O
CO32-+H+£¬HCO3-+H2O H2CO3+OH-£¬
H2CO3+OH-£¬ CO32-+H+£¬HCO3-+H2O
CO32-+H+£¬HCO3-+H2O H2CO3+OH-£¬
H2CO3+OH-£¬²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŌĶĮĄķ½ā
 £Ø1£©øĒĖ¹¶ØĀÉČĻĪŖ£ŗ²»¹Ü»Æѧ¹ż³ĢŹĒŅ»²½Ķź³É»ņ·ÖŹż²½Ķź³É£¬Õūøö¹ż³ĢµÄ×Ü
£Ø1£©øĒĖ¹¶ØĀÉČĻĪŖ£ŗ²»¹Ü»Æѧ¹ż³ĢŹĒŅ»²½Ķź³É»ņ·ÖŹż²½Ķź³É£¬Õūøö¹ż³ĢµÄ×ܲéæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com