
某溶液中滴入BaCl2溶液,产生白色沉淀,再滴入稀盐酸,沉淀不溶解,则该溶液中
A. 一定有SO42- B. 可能有SO42- 或Ag+
C. 一定无Ag+ D. 还可能有CO32-
 全优点练单元计划系列答案
全优点练单元计划系列答案科目:高中化学 来源: 题型:
CuI是一种不溶于水的白色固体,它可以由反应:2Cu2++4I-===2CuI↓+I2而得到。如图所示装置中,a、b都是惰性电极,通电一段时间后,在KI淀粉溶液中阳极周围变蓝色,则下列说法正确的是( )
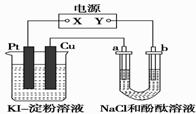
A.若a极变红,则在Pt电极上:2I--2e-===I2,淀粉遇碘变蓝
B.若b极变红,则在Pt电极上:4OH--4e-===2H2O+O2↑,O2将I-氧化为I2,淀粉遇碘变蓝
C.若a极变红,则在Cu电极上:2Cu+4I--4e-===2CuI↓+I2,碘遇淀粉变蓝
D.若b极变红,则在Cu极上:Cu-2e-===Cu2+,Cu2+显蓝色
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关物质的性质和应用均正确的是 ( )
A.NH3能氧化氮氧化物,可用于汽车尾气净化
B.Mg、Fe等金属在一定条件下与水反应都生成H2和对应的氢氧化物
C.Fe在O2中的燃烧产物可用于制红色涂料
D.Mg (OH)2分解吸热且生成高熔点固体,可用作阻燃剂
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42-、HCO3-等离子。当向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀物质的量随NaOH溶液的体积变化的图象如图所示,下列说法正确的是( )
A.原溶液中含有的Fe3+和Al3+的物质的量之比为1:1
B.ab段发生的离子反应为:Al3++3OH-= Al(OH)3↓,Mg2++2OH-= Mg(OH)2↓
C.原溶液中含有的阳离子是H+、NH4+、Mg2+、Al3+、Na+
D.d点溶液中含有的溶质只有Na2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
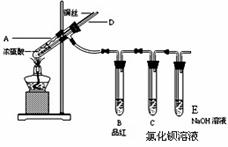 某实验小组同学为了探究铜与浓硫酸的反应,进行如下实验。
某实验小组同学为了探究铜与浓硫酸的反应,进行如下实验。
实验1:铜与浓硫酸反应,实验装置如图所示。
实验步骤:
①先连接好装置,检验气密性,加入试剂;
②加热A试管直到B中品红褪色,熄灭酒精灯;
③将Cu丝上提离开液面;
(1)能够证明铜与浓硫酸反应产生的气体的现象: 。
(2)在盛有氯化钡溶液的C试管中除了导管口有气泡外,无其他明显现象,若将其分为两份,分别滴加下列溶液,将产生沉淀的化学式填入下表相应位置。
| 滴加的溶液 | 氯水 | 氨水 |
| 沉淀的化学式 | __________________________ | __________________________ |
写出其中SO2显示还原性的离子方程式: 。
(3)熄灭酒精灯后,因为有导管D的存在,B中的液体不会倒吸,
其原因是: 。
(4)将SO2气体通入含有n mol Na2S溶液中,溶液中出现黄色浑浊,试分析该溶液最多能吸收SO2气体 mol。 (不考虑溶解的SO2)。
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液中只含有K+ 、Na+ 、NO3- 、SO42-等四种离子,它们的物质
的量之比为1∶6∶3∶2该溶液所含的溶质可能是( )
A、KNO3、Na2SO4 B、K2SO4、NaNO3、KNO3
C、KNO3 、Na2SO4、NaNO3 D、K2SO4、Na2SO4、KNO3、
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)9.2g氮的氧化物NOx中含有N原子数为0.2 mol,
则NOx的摩尔质量为___________,x数值为_______,
这些质量的NOx在标准状况的体积约为_______。
(2)V L Fe2(SO4)3溶液中含有a g SO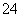 ,取此溶液0.5V L,用水稀释至2V L,则稀释后溶液中Fe3+的物质的量的浓度为_________________
,取此溶液0.5V L,用水稀释至2V L,则稀释后溶液中Fe3+的物质的量的浓度为_________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【化学——选修5:有机化学基础】(15分)
白酒产品中的塑化剂主要源于塑料接酒桶、塑料输酒管、成品酒塑料内盖等。DBP是塑化剂的一种,可由下列路线合成:
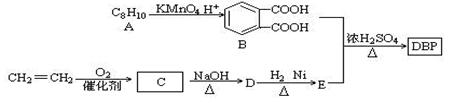
已知以下信息:
①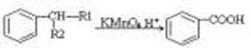
②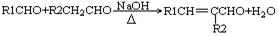
(-R1、-R2表示氢原子或烃基)
(1)A的结构简式 ,D的结构简式是 ,
D→E的反应类型 。
(2)D和H2 1︰1反应生成E,则E官能团名称为_________,DBP的分子式为 .(3)由B和E以物质的量比1︰2合成DBP的化学方程式: 。
(4)写出同时符合下列条件的B的所有同分异构体结构简式 。
①能和NaHCO3溶液反应生成CO2 ③能使FeC13溶液发生显色反应
②能发生银镜反应 ④苯环上含碳基团处于对位
(5)写出B与碳酸氢钠溶液反应的方程式 。
写出C生成D的反应的方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
科学家一直致力于研究常温、常压下“人工固氮”的新方法。曾有实验报道:在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生反应,生成的主要产物为NH3。进一步研究NH3生成量与温度的关系,部分实验数据见下表(光照、N2、压强1.0×105 Pa、反应时间3 h):
| T/K | 303 | 313 | 323 | 353 |
| NH3生成量 /10-6 mol | 4.8 | 5.9 | 6.0 | 2.0 |
相应的热化学方程式如下:N2(g)+3H2O(l)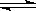 2NH3(g)+
2NH3(g)+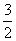 O2(g)
O2(g)
ΔH=+765.2 kJ·mol-1
回答下列问题:(1)请画出上述反应在有催化剂与无催化剂两种情况下反应过程中体系能量变化的示意图,并进行必要标注。
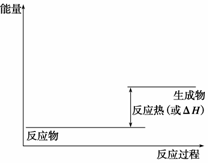
(2)与目前广泛使用的工业合成氨方法相比,该方法固氮反应速率慢。请提出可提高其反应速率且增大NH3生成量的建议:(写两点)
_______________________________;____________________________________。
(3)工业合成氨的反应为N2(g)+3H2(g) 2NH3(g)。设在容积为2.0 L的密闭容器中充入0.60 mol N2(g)和1.60 mol H2(g),反应在一定条件下达到平衡时,NH3的物质的量分数(NH3的物质的量与反应体系中总的物质的量之比)为
2NH3(g)。设在容积为2.0 L的密闭容器中充入0.60 mol N2(g)和1.60 mol H2(g),反应在一定条件下达到平衡时,NH3的物质的量分数(NH3的物质的量与反应体系中总的物质的量之比)为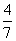 。计算:①该条件下N2的平衡转化率为 (保留一位小数)。
。计算:①该条件下N2的平衡转化率为 (保留一位小数)。
②该条件下反应2NH3(g) N2(g)+3H2(g)的平衡常数 。
N2(g)+3H2(g)的平衡常数 。
③若反应温度不变,假如在容积为2.0 L的密闭容器中起始充入0.40 mol N2(g)和0.40 mol H2(g),反应3min时测得体系压强为原来的3/4,这段时间H2的平均反应速率为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com