
分析 (1)由①N2(g)+2O2(g)═2NO2(g)△H=+akJ/mol
②N2H4(g)+O2(g)═N2(g)+2H2O(g)△H=-b kJ/mol
③2NO2(g?N2O4(g)△H=-ckJ/mol
根据盖斯定律可知②×2-①-③得热化学方程式;
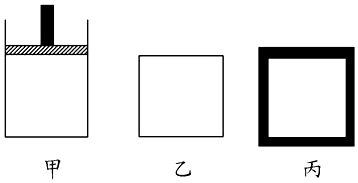
(2)①甲乙容器温度不变,平衡常数不变,丙容器绝热,温度升高平衡逆向进行,平衡常数减小;
②乙容器保持体积不变,随着反应的进行,压强减小,甲容器在反应过程中保持压强不变,故甲对于乙来说,相当于增大压强,平衡正向移动;丙容器绝热,温度升高平衡逆向进行;
③A.总质量一定,体积一定,故乙容器气体密度不再变化时,不能说明此反应已达到平衡状态;
B.在甲中充入稀有气体He,体积增大,原体系的压强减小,化学反应速率减慢;
C.向甲容器中冲入氨气,体积增大,氢气和氮气的浓度减小,氨气的浓度增大,故正向速率减小,逆向速率增大;
D.丙容器绝热,故丙容器温度不再变化时说明已达平衡状态.
解答 解:(1)由①N2(g)+2O2(g)═2NO2(g)△H=+akJ/mol
②N2H4(g)+O2(g)═N2(g)+2H2O(g)△H=-b kJ/mol
③2NO2(g?N2O4(g)△H=-ckJ/mol
根据盖斯定律可知②×2-①-③得2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g),△H=-(a-c+2b)kJ/mol,
故答案为:2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g),△H=-(a-c+2b)kJ/mol;
(2)①甲乙容器温度不变,平衡常数不变,丙容器绝热,温度升高平衡逆向进行,平衡常数减小,故K甲=K乙>K丙;
故答案为:=,>;
②甲容器在反应过程中保持压强不变,故容器体积减小,氮气的浓度增大;乙容器保持体积不变,随着反应的进行,压强减小;丙容器绝热,温度升高平衡逆向进行,故达到平衡时N2的浓度c(N2)甲>c(N2)乙<c(N2)丙,
故答案为:>,<;
③A.总质量一定,体积一定,故乙容器气体密度不再变化时,不能说明此反应已达到平衡状态,故A错误;
B.在甲中充入稀有气体He,体积增大,原体系的压强减小,化学反应速率减慢,故B错误;
C.向甲容器中冲入氨气,体积增大,氢气和氮气的浓度减小,氨气的浓度增大,故正向速率减小,逆向速率增大,故C正确;
D.丙容器绝热,故丙容器温度不再变化时说明已达平衡状态,故D正确;
故答案为:CD.
点评 本题考查的知识点较多,为高考常见题型,侧重于学生的分析能力的考题,题目涉及盖斯定律的应用、化学方程式、化学反应速率和化学平衡的相关知识,难度较大.


 口算能手系列答案
口算能手系列答案科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 编号 | 实验 | 操作 |
| A | 实验室用自来水制备蒸馏水 | 将自来水倒入烧杯中,小心给烧杯加热 |
| B | 配制一定浓度的氯化钾溶液100mL | 将称好的氯化钾固体放入100mL容量瓶中,加水溶解,振荡摇匀,定容 |
| C | 检验溶液中是否含SO42- | 先加入稀盐酸,无明显现象,再加入BaCl2溶液 |
| D | 取出分液漏斗中的上层液体 | 下层液体从分液漏斗下端管口放出,关闭活塞,换一个接收容器,上层液体继续从分液漏斗下端管口放出 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,11.2LH2O 含有的分子数为0.5NA | |
| B. | 在常温常压下,11.2LCl2含有的分子数为0.5NA | |
| C. | 含有NA个氩原子的氩气在标准状况下的体积约为11.2L | |
| D. | 25℃,1.01×105 Pa,64gSO2中含有的原子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe分别与氯气和稀盐酸反应所得氯化物相同 | |
| B. | K、Zn分别与不足量的稀硫酸反应所得溶液均呈中性 | |
| C. | Li、Na、K的原子半径和密度随原子序数的增加而增大 | |
| D. | C、S、Cl的最高价氧化物对应水化物的酸性逐渐增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用食醋清洗热水瓶中的水垢【主要成分是CaCO3和Mg(OH)2】 | |
| B. | 用煤气灶燃烧天然气为炒菜提供热量 | |
| C. | 烧菜用过的铁锅,经放置常出现红棕色斑迹 | |
| D. | 牛奶久置变质腐败 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com