
分析 (1)单质是只由一种元素构成的纯净物,而做防腐剂的物质必须自身性质较稳定且无毒;
(2)盐是阳离子是金属离子或铵根离子,阴离子是酸根离子的化合物,而铵盐可以作为化肥;
(3)氧化物是由两种元素构成,其中一种是氧元素的化合物,且该氧化物为碱性氧化物;
(4)碱是电离出的阴离子全部是OH-的化合物,除了NaOH、KOH、Ba(OH)2、NH3•H2O易溶于水,而Ca(OH)2微溶于水,其他的碱均难溶于水;
解答 解:(1)氮气的化学性质比较稳定,可以用作食品防腐剂;
(2)氯化铵中含有氮元素,是一种常见的氮肥;
(3)氧化钙可以与酸反应,故可用于改良酸性土壤;
(4)氢氧化铁是一种不溶于水的红褐色沉淀;
故答案为:(1)N2;(2)NH4Cl;(3)CaO;(4)Fe(OH)3.
点评 本题难度不大,熟练掌握常见物质的性质、分类、用途、组成及化学式的书写是正确解答此类题的关键所在.


 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案科目:高中化学 来源: 题型:选择题
| A. | 离子化合物中一定不含共价键,共价化合物中一定不含离子键 | |
| B. | 两种微粒,若核外电子排布完全相同,则其化学性质一定相同 | |
| C. | 碳原子之间可形成碳碳单键、碳碳双键或碳碳叁键 | |
| D. | 分子间作用力越大,分子的热稳定性就越大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
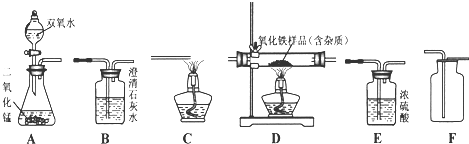
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸能使紫色石蕊试液变红,二氧化碳也能使紫色石蕊变红,所以二氧化碳是酸 | |
| B. | 某物质在空气中燃烧后生成二氧化碳和水,则该物质中一定含有氧元素 | |
| C. | 向某溶液中滴加氯化钡溶液,产生不溶于稀硝酸的白色沉淀,说明该溶液中可能存在SO42- | |
| D. | 溶液中有晶体析出,其溶质的质量减少,所以溶质的质量分数一定减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
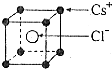
| A. | $\frac{8M}{{N}_{A}•{a}^{3}}$ | B. | $\frac{6M}{{N}_{A}•{a}^{3}}$ | C. | $\frac{4M}{{N}_{A}•{a}^{3}}$ | D. | $\frac{M}{{N}_{A}•{a}^{3}}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C8H16与甲烷互为同系物 | |
| B. | 乙烯只能加成、不能取代,苯只能取代、不能加成 | |
| C. | CH3CH2CH2CH3和 互为同分异构体 互为同分异构体 | |
| D. |  和 和 互为同分异构体 互为同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 吸氢材料镧镍合金 | B. | 半导体材料砷化镓 | ||
| C. | 高温结构陶瓷材料氮化硅 | D. | 透明陶瓷材料硒化锌 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com