
| A. | NCl3为非极性分子 | |
| B. | NCl3跟水反应的产物为NH3和HClO | |
| C. | NCl3跟水反应生成NH4Cl、O2和Cl2 | |
| D. | 在NCl3分子中N为+3价,跟水发生水解反应的产物是HNO2和HCl |
分析 A.NCl3的分子空间构型与氨分子相似,都是三角锥型结构;
B.与水反应不存在化合价变化;
C.与水反应不存在元素的化合价变化;
D.氮与氯的共用电子对偏向氮原子,N显负价.
解答 解:A.因氨气分子的空间构型推知NCl3为三角锥形结构,为极性分子,故A错误;
B.因氮与氯的共用电子对偏向氮原子,则在NCl3中,N显-3价,Cl显+1价,则其发生水解的方程式应为NCl3+3H2O═NH3+3HClO,故B正确;
C.由选项C可知,水解的方程式应为NCl3+3H2O═NH3+3HClO,故C错误;
D.氮与氯的共用电子对偏向氮原子,N显-3价,Cl显+1价,水解的方程式应为NCl3+3H2O═NH3+3HClO,故D错误;
故选B.
点评 本题考查物质的性质及水解反应,为高频考点,把握物质的性质、习题中的信息判断水解反应为解答的关键,侧重分析与应用能力的考查,注意氮与氯的共用电子对偏向氮原子,题目难度不大.


科目:高中化学 来源: 题型:解答题
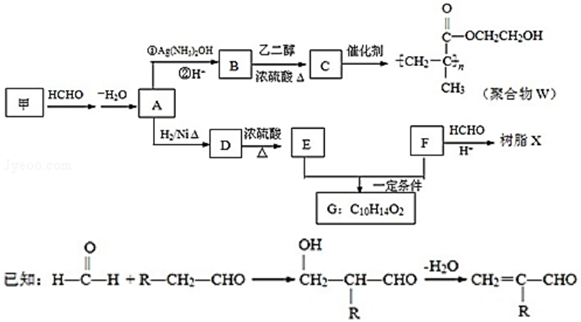
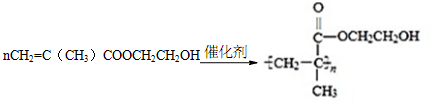 .
.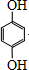
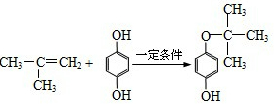 ,反应类型是加成反应.
,反应类型是加成反应.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Na2O>Na2O2 | B. | Na2CO3>NaHCO3>H2CO3 | ||
| C. | Na2SO4•10H2O>Na2CO3•10H2O | D. | NaClO>NaCl>NaF |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用小苏打治疗胃酸过多:HCO3-+H+═CO2↑+H2O | |
| B. | Ca(HCO3)2溶液与过量NaOH溶液反应:HCO3-+OH-═CO32-+H2O | |
| C. | 利用腐蚀法制作印刷线路板:Fe3++Cu═Fe2++Cu2+ | |
| D. | 钠与水反应:Na+H2O═Na++OH-+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.3 mol/L Na2SO4溶液中含有Na+和SO42-总物质的量为0.9mol | |
| B. | 当1L水吸收22.4LNH3时所得氨水的浓度不是1 mol/L,只有当22.4L NH3溶于水制得1L氨水时,其浓度才是1 mol/L | |
| C. | 10℃时0.5 mol/L的稀盐酸100mL,蒸发掉5g水,冷却到10℃时,其体积小于100mL,它的物质的量浓度大于0.5 mol/L | |
| D. | 10℃时0.5 mol/L的KCl饱和溶液100mL,蒸发掉5g水,冷却到10℃时,其体积小于100 mL,它的物质的量浓度仍为0.5 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com