目前正在研究和已经使用的储氢合金有镁系合金、稀土系合金等.
(1)已知:Mg(s)+H
2(g)=MgH
2(s)△H
1=-74.5kJ?mol
-1Mg
2Ni(s)+2H
2(g)=Mg
2NiH
4(s)△H
2=-64.4kJ?mol
-1Mg
2Ni(s)+2MgH
2(s)=2Mg(s)+Mg
2NiH
4(s)△H
3,则△H
3=
kJ?mol
-1.
(2)工业上用电解熔融的无水氯化镁获得镁.其中氯化镁晶体脱水是关键工艺之一,
一种氯化镁晶体脱水的方法是:先将MgCl
2?6H
2O转化为MgCl
2?NH
4C1?nNH
3(铵镁复盐),然后在700℃脱氨得到无水氯化镁,脱氨反应的化学方程式为
.
(3)储氢材料Mg(AlH
4)
2在110~200℃的反应为:Mg(AlH
4)
2=MgH
2+2Al+3H
2↑.生成2.7gAl时,产生的H
2在标准状况下的体积为
L.
(4)采用球磨法制备Al与LiBH
4的复合材料,并对Al-LiBH
4体系与水反应产氢的特性进行下列研究:
①如图1为25℃水浴时每克不同配比的Al-LiBH
4复合材料与水反应产生H
2体积随时间变化关系图.由图可知,下列说法正确的是
(填字母).
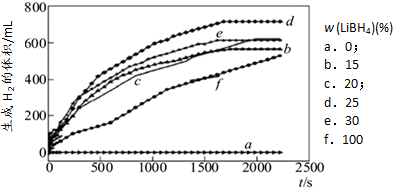
a.25℃时,纯铝与水不反应
b.25℃时,纯LiBH
4与水反应产生氢气
c.25℃时,Al-LiBH
4复合材料中LiBH
4含量越高,1000s内产生氢气的体积越大
②如2图为25℃和75℃时,Al-LiBH
4复合材料[w (LiBH
4)=25%]与水反应一定时间后产物的X-射线衍射图谱(X-射线衍射可用于判断某晶态物质是否存在,不同晶态物质出现衍射峰的衍射角不同).
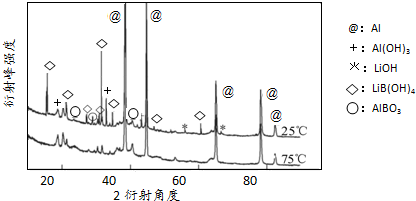
从图中可知,25℃时Al-LiBH
4复合材料中与水完全反应的物质是
(填化学式).
(5)储氢还可借助有机物,如利用环己烷和苯之间的可逆反应来实现脱氢和加氢:
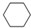
(g)
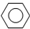
(g)+)+3H
2(g)
①某温度下,向恒容密闭容器中加入环己烷,起始浓度为a mol?L
-1,平衡时苯的浓度为b mol?L
-1,该反应的平衡常数K=
.
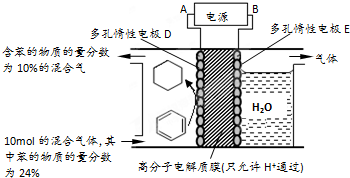
②一定条件下,如图3装置可实现有机物的电化学储氢(忽略其它有机物).生成目标产物的电极反应式为
.



 (g)
(g) (g)+)+3H2(g)
(g)+)+3H2(g)


 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案 (1)已知:常压下,氨气在300℃时约有9.7%分解,水蒸气在2000℃时约有4%分解,氟化氢气体在3000℃时仍不分解.这三种分子的中心原子与氢原子形成的σ键能由大到小的顺序是
(1)已知:常压下,氨气在300℃时约有9.7%分解,水蒸气在2000℃时约有4%分解,氟化氢气体在3000℃时仍不分解.这三种分子的中心原子与氢原子形成的σ键能由大到小的顺序是