
【题目】利用如图所示的实验装置进行实验。
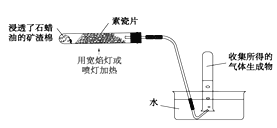
(1)装置中素瓷片的作用____________,矿渣棉的作用__________。
(2)请设计实验证明所得气体生成物中含有不饱和气态烃______。
【答案】作催化剂 作为石蜡油的载体 将所得气体通入到酸性高锰酸钾溶液或溴水溶液中,若观察到溶液颜色褪色则说明所得气体中含有气态不饱和烃
【解析】
石蜡油主要含碳、氢元素,经过反应产生能使酸性高锰酸钾溶液褪色的气体,一般是气态不饱和烃,如乙烯或乙炔等。石蜡油分子本身碳原子数较多,经过反应产生乙烯、乙炔等小分子,主要是发生了催化裂化,生成相对分子质量较小、沸点较低的烃。
(1)根据上述分析可知:装置中素瓷片起到了催化剂的作用,矿渣棉用作为石蜡油的载体,故答案:作催化剂;作为石蜡油的载体;
(2)因为石蜡油主要含碳、氢元素,主要是发生了催化裂化,经过反应能生成气态不饱和烃,如乙烯或乙炔等。这些气态不饱和烃能使酸性高锰酸钾溶液褪色,也可以和溴水发生加成反应,所以可以将所得气体通入到酸性高锰酸钾溶液或溴水溶液中,若观察到溶液颜色褪色则说明所得气体中含有气态不饱和烃,故答案:将所得气体通入到酸性高锰酸钾溶液或溴水溶液中,若观察到溶液颜色褪色则说明所得气体中含有气态不饱和烃。


 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案科目:高中化学 来源: 题型:
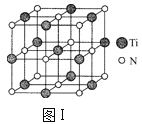
【题目】(1)以四氯化钛、碳化钙、叠氮酸盐作原料,可以生成碳氮化钛化合物。其结构是用碳原子取代氮化钛晶胞(结构如图Ⅰ)顶点的氮原子,这种碳氮化钛化合物的化学式为___。
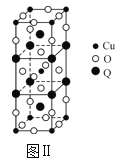
(2)图Ⅱ是由Q、Cu、O三种元素组成的一种高温超导体的晶胞结构,其中Cu为+2价,O为-2价,则Q的化合价为___价。
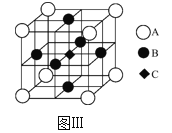
(3)一种新型阳极材料LaCrO3的晶胞如图Ⅲ所示,已知距离每个Cr原子最近的原子有6个,则图Ⅲ中___(填字母)原子代表的是Cr原子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据要求完成下列实验。(a、b为弹簧夹,其他装置略去)
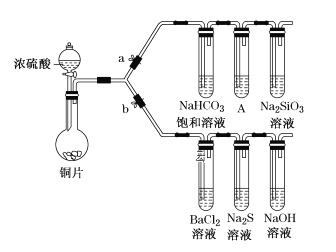
Ⅰ.验证酸性的相对强弱:碳酸>硅酸。(已知酸性:亚硫酸>碳酸)
(1)铜与浓硫酸反应的化学方程式是________________,装置A中的足量的试剂是________________。
(2)连接仪器、__________、加药品后,打开a关闭b,然后滴入浓硫酸,加热。能说明碳酸的酸性比硅酸酸性强的实验现象是__________________。
Ⅱ.验证SO2具有氧化性、还原性和酸性氧化物的通性。
(3)打开b,关闭a,能验证SO2具有氧化性的化学方程式是________________
(4)若过量的SO2通入NaOH溶液中,其化学方程式是____。
(5)BaCl2溶液中无任何现象,将其分成两份,分别滴加氨水和氯水,均产生白色沉淀,沉淀化学式是_____________________。其中SO2显示还原性并生成白色沉淀的总的离子方程式:______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,将CuSO4·5H2O(s)溶于水会使溶液温度降低,将 CuSO4(s)溶于水会使溶液温度升高。则下列能量转化关系不正确的是
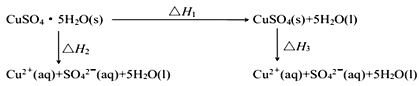
A.ΔH1>0B.ΔH2<ΔH3C.ΔH3<ΔH1D.ΔH2=ΔH1+ΔH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组以石膏(CaSO4·2H2O)为主要原料制备(NH4)2SO4的流程如下:
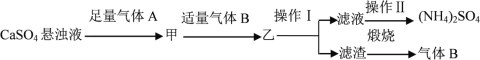
下列说法正确的是
A.气体A是CO2,气体B是NH3
B.操作Ⅰ中,所用的主要玻璃仪器为烧杯、玻璃棒、分液漏斗
C.操作Ⅱ中,将滤液加热蒸干并灼烧可以得到纯净的(NH4)2SO4
D.整个过程的总反应方程式为CaSO4+CO2+2NH3+H2O=CaCO3↓+(NH4)2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以天然气为原料合成氨是现代合成氨工业发展的方向与趋势
(一)天然气与氮气为原料,以固态质子交换膜为电解质,在低温常压下通过电解原理制备氨气如图所示:
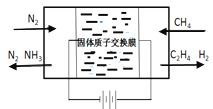
写出在阴极表面发生的电极反应式:_____________。
(二)天然气为原料合成氨技术简易流程如下:

一段转化主要发生的反应如下:
①CH4(g) +H2O(g) ![]() CO(g)+3H2(g) ΔH1 = 206 kJ·molˉ1
CO(g)+3H2(g) ΔH1 = 206 kJ·molˉ1
②CO(g) + H2O(g) ![]() CO2(g) + H2(g) ΔH2 = -41 kJ·molˉ1
CO2(g) + H2(g) ΔH2 = -41 kJ·molˉ1
二段转化主要发生的反应如下:
③2CH4(g)+ O2(g) ![]() 2CO(g)+4H2(g) ΔH3 = -71.2 kJ·molˉ1
2CO(g)+4H2(g) ΔH3 = -71.2 kJ·molˉ1
④2CO(g) + O2(g) ![]() 2CO2(g) ΔH4 = -282 kJ·molˉ1
2CO2(g) ΔH4 = -282 kJ·molˉ1
(1)已知CO中不含C=O,H-H的键能为436 kJ·molˉ1,H-O的键能为463 kJ·molˉ1,C-H的键能为414 kJ·molˉ1,试计算C=O的键能_________。
(2)实验室模拟一段转化过程,在800oC下,向体积为1L的恒容密闭反应器中,充入1mol的CH4与1mol的H2O,达到平衡时CH4的转化率为40%,n(H2)为1.4mol,请计算反应②的平衡常数_________。
(3)下列说法正确的是_________。
A.合成氨过程实际选择的温度约为700℃,温度过高或过低都会降低氨气平衡产率
B.上述工业流程中压缩既能提高反应速率又能提高合成氨的产率
C.二段转化释放的热量可为一段转化提供热源,实现能量充分利用
D.二段转化过程中,需严格控制空气的进气量,否则会破坏合成气中的氢氮比
(4)已知催化合成氨中催化剂的活性与催化剂的负载量、催化剂的比表面积和催化反应温度等因素有关,如图所示:

①实验表明相同温度下,负载量5%催化剂活性最好,分析负载量9%与负载量1%时,催化剂活性均下降的可能原因是________。
②在上图中用虚线作出负载量为3%的催化剂活性变化曲线_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向20 mL某浓度的AlCl3溶液中滴加2 mol·L-1的NaOH溶液时,得到Al(OH)3沉淀的质量(g)与所滴加NaOH溶液的体积(mL)关系如图所示,试回答下列问题:
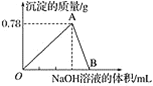
(1)图中A点表示的沉淀是__________(写化学式),其物质的量为____________。
(2)反应至A点时消耗NaOH溶液的体积为______________。
(3)图中B点溶液中的溶质有________________。
(4)AlCl3溶液的浓度为______________。
(5)O点到B点反应的总离子方程式可表示为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某柔性屏手机的柔性电池以碳纳米管做电极材料,以吸收ZnSO4溶液的有机高聚物做固态电解质,其电池总反应为:MnO2+ Zn + (1+x/6) H2O + ZnSO4![]() MnOOH + ZnSO4[Zn(OH)2]3·xH2O其电池结构如图1所示,图2是有机高聚物的结构片段。下列说法中,不正确的是( )
MnOOH + ZnSO4[Zn(OH)2]3·xH2O其电池结构如图1所示,图2是有机高聚物的结构片段。下列说法中,不正确的是( )

A.碳纳米管具有导电性,可用作电极材料
B.放电时,电池的正极反应为:MnO2 + e + H+ == MnOOH
C.充电时,Zn2+移向Zn膜
D.有机高聚物是一种混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物W的分子式为C9H12 ,其含有苯环的结构有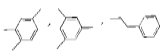 等,下列说法错误的是( )
等,下列说法错误的是( )
A. ![]() 与苯互为同系物
与苯互为同系物
B. 除了上述三种物质,W的含苯环的同分异构体还有5种
C. 有机物W的一种结构为![]() 该有机物不能与溴单质发生加成反应
该有机物不能与溴单质发生加成反应
D. 有机物W不管是否含有苯环,在一定条件下都能发生氧化反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com