
| A、O3和O2互为同位素 |
| B、O3比O2稳定 |
| C、等质量的O3和O2含有相同的原子数 |
| D、O3与O2的相互转变是物理变化 |


 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:
 在密闭容器中进行反应CH4(g)+H20(g)?CO(g)+3H2(g)△H>0测得c(CH4)随反应时间(t)的变化如图所示.下列判断正确的是( )
在密闭容器中进行反应CH4(g)+H20(g)?CO(g)+3H2(g)△H>0测得c(CH4)随反应时间(t)的变化如图所示.下列判断正确的是( )| A、10 min时,改变的外界条件可能是温度 |
| B、0~5 min内,V(H2)=0.1 mol?L-1?min-1 |
| C、恒温下,缩小容器体积,平衡后c(H2)肯定减小 |
| D、10-12 min时反应的平衡常数逐渐增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、立即关闭大门,躲到床下 |
| B、伏倒在地,观察情况变化 |
| C、冲出家门,向洼地转移 |
| D、用湿毛巾捂住口腔和鼻子,朝上风口走,迅速离开村子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 向50mL NaOH溶液中逐渐通入一定量的CO2(假设溶液体积不变),随后取此溶液10mL,将其稀释至100mL,并向此稀释后的溶液中逐滴加入0.1mol?L-1的盐酸,产生CO2气体的体积(标准状况下)与所加入的盐酸的体积关系如图,下列分析错误的是( )
向50mL NaOH溶液中逐渐通入一定量的CO2(假设溶液体积不变),随后取此溶液10mL,将其稀释至100mL,并向此稀释后的溶液中逐滴加入0.1mol?L-1的盐酸,产生CO2气体的体积(标准状况下)与所加入的盐酸的体积关系如图,下列分析错误的是( )| A、OA段所发生反应的离子方程式:H++OH-═H2O、CO32-+H+═HCO3- |
| B、NaOH在吸收CO2后,所得溶液的溶质为NaOH和Na2CO3,其物质的量浓度之比为1:1 |
| C、原NaOH溶液的物质的量浓度为0.5 mol?L-1 |
| D、标准状况下产生CO2气体的体积为56mL |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 化学方程式 | K(t1) | K(t2) |
| F2+H2?2HF | 1.8×1036 | 1.9×1032 |
| Cl2+H2?2HCl | 9.7×1012 | 4.2×1011 |
| Br2+H2?2HBr | 5.6×107 | 9.3×106 |
| I2+H2?2HI | 43 | 34 |
查看答案和解析>>
科目:高中化学 来源: 题型:
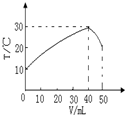 向盛有50mL1.00mol?L-1HCl溶液的绝热容器中加入NaOH溶液,NaOH溶液的体积(V)与所得混合溶液的最高测量温度(T)的关系如图所示,下列不正确的是( )
向盛有50mL1.00mol?L-1HCl溶液的绝热容器中加入NaOH溶液,NaOH溶液的体积(V)与所得混合溶液的最高测量温度(T)的关系如图所示,下列不正确的是( )| A、该实验表明化学能可以转化为热能 |
| B、NaOH溶液的浓度大于1.00mol?L-1 |
| C、V=50mL时,混合液的pH>7 |
| D、该实验表明有水生成的反应都是放热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com