
����Ŀ���⻯�(LiH)�ڸ���Ŀ��������ȶ����ڣ���ˮ�����ܹ�����ȼ�ա�ij�С����ʹ������װ���Ʊ�LiH���塣
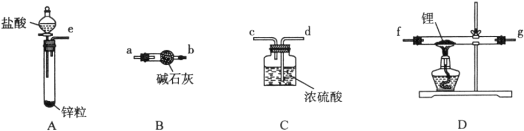
��ͬѧ��ʵ�鷽�����£�
��1����������װ���ӣ���������װ�ýӿڵ�����˳��Ϊ____________________������ҩƷǰ����Ҫ���е�ʵ�������____________________(����д������IJ�������)������װ��B��������________________��
��2������ҩƷ�������Ӵ��Լ�ƿ��ȡ��һ���������(����ʯ���ܷ�)��Ȼ���ڼױ��н�ϴ���Σ��ò�����Ŀ����________________________________________��Ȼ����ٰ�﮷��뵽ʯӢ���С�
��3��ͨ��һ��ʱ�����������ʯӢ�ܣ��ڼ���D����ʯӢ��֮ǰ��������е�ʵ�������______________________________________________________________________��
��4������һ��ʱ���ֹͣ���ȣ�����ͨ������ȴ��Ȼ��ȡ��LiH��װ�뵪���ƿ������ڰ�������ȡ����������Ŀ����Ϊ�˱���LiH������е�ˮ�����Ӵ�������Σ�ա�(��Ӧ����ʽ��
LiH + H2O = LiOH + H2��)�������÷�Ӧԭ�������LiH����ˮ�Ҵ���Ӧ�Ļ�ѧ����ʽ_________________ ___________________��
��5��ȷ�����ƵõIJ�Ʒ0.174g����һ��������������ˮ��Ӧ���ռ�������0.021mol�����Ʒ��LiH��Li�����ʵ���֮��Ϊ____________________��
��6����ͬѧ�Լ�ʵ�鷽��������ɣ�����Ϊδ��Ӧ��H2����ֱ���ŷţ����������������װ��E�����ռ�H2���뽫Eװ�ò���������
���𰸡���1��eabfgdc (f��g����Ҳ����)�� ����װ�õ������� ��ȥH2�е�H2O��HCl
��2����ȥﮱ����ʯ����3���ռ�c���ų������岢����H2���� (ֻд����H2����Ҳ����)
��4��LiH + CH3CH2OH ![]() CH3CH2OLi + H2����5��10��1
CH3CH2OLi + H2����5��10��1
��6��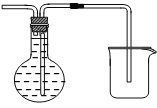
��������
�����������1��������﮷�����Ӧ����LiH���Ʊ�LiH������Ҫ�Ʊ�������LiH�ڸ���Ŀ��������ȶ����ڣ���ˮ�����ܹ�����ȼ�գ������Ʊ��õ�������������﴿��������Aװ���Ʊ���������װ��B�еļ�ʯ�ҳ�ȥ�����е��Ȼ����ˮ������ͨ��װ��D�м��Ⱥ�﮷�Ӧ�����⻯ﮣ��������װ��C����ֹ�����е�ˮ�����Ͷ�����̼����װ��D�����ɵ��⻯﮷�����Ӧ��װ������˳��Ϊ��e��a��b��f��g��d���Ʊ�����װ�ã�����ҩƷǰ����Ҫ���е�ʵ������ǣ�����װ�������ԣ�װ��B�м�ʯ���������ƺ��������ƵĻ�����������ˮ�ɷ�Ӧ���������ƿ�������������������ܷ�Ӧ�����Ը�װ�õ�����������ˮ�����Ͳ����Ȼ������壬�ʴ�Ϊ��e��a��b��f��g��d������װ�������ԣ���ȥH2�е�H2O��HCl��
��2��ȡ��һ���������(����ʯ���ܷ�)��Ȼ���ڼױ��н�ϴ���Σ�����ʯ�����л������ܽ����л��ܼ��ױ��У�������Ŀ���dz�ȥﮱ����ʯ�����ʴ�Ϊ����ȥﮱ����ʯ����
��3��ʹ��ǰӦͨ��һ��ʱ���������ž�װ���ڵĿ�������ֹ����ʱ��������������ըΣ�գ��ڼ���D����ʯӢ��֮ǰ��������е�ʵ������ǣ��ռ�c���ų������岢����H2���ȣ��ʴ�Ϊ���ռ�c���ų������岢����H2���ȣ�
��4��LiH��H2O����ˮ�ⷴӦ������ӽ�����������ӣ��⸺�����������ӽṹ����������LiH���Ҵ���Ӧ���ƣ��ǻ��ṩHԭ����LiH��Ӧ�������������ⲿ�ֽ������CH3CH2OLi����Ӧ����ʽΪ��LiH+CH3CH2OH=CH3CH2OLi+H2�����ʴ�Ϊ��LiH+CH3CH2OH=CH3CH2OLi+H2����
��5����LiH��Li�����ʵ����ֱ�Ϊxmol��ymol����
LiH+H2O=H2��+LiOH
xmol xmol
2Li+2H2O=2LiOH+H2��
ymol 0.5y mol
��8x+7y��0.174��22.4(x+0.5y)��0.4704��
���x=0.02��y=0.002
��LiH��Li�����ʵ���֮��Ϊ0.02mol:0.002mol=10:1���ʴ�Ϊ��10:1��
��6��װ��E�����ռ�H2�����õ�������ƿ���ռ����������Ը�����ˮ���������װ�ã������ܶ̽�������װ��ͼΪ ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��


 ��Ȥ������ҵ���ϿƼ�������ϵ�д�
��Ȥ������ҵ���ϿƼ�������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�ִ�����ˮ��ȼ�ϵ��ģ������ͼ��ʾ���õ�ع���ʱ��ֻ�����ˮע�뷴Ӧ�أ�ϸ���Ϳɽ���ˮ�е��л���ֽ⣬�ڴ˹������ͷų����ӡ����Ӻ��ҡ�������������ȷ����
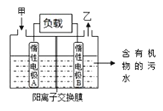
A��B�缫Ϊ����
B�������ҿ���ΪCO2
C��O2��A�缫�õ���
D����ع���ʱ��B�缫������pH��С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��������ͨ����������S8(б����)����ʽ���ڣ���������״̬ʱ������S2��S4��S6��S8�ȶ���ͬ�������壬����S4��S6��S8�������ƵĽṹ�ص㣬��ṹ����ͼ��ʾ��

�ش��������⣺
��1�������й�˵����ȷ���� ��
A.S2��S4��S6��S8��Ϊͬϵ�� B.S8ת��ΪS6��S4��S2���������仯
C.������������ӣ���ȫȼ��ʱ������SO2 D.���������µ�����Ϊԭ�Ӿ���
E.32gS8�������е�S��S������ΪNA
��2����һ���¶��£������������ƽ��Ħ������Ϊ80g/mol�����������S2���ӵ����������С�� ��
��3����һ�������£�S8(s)��O2(g)������Ӧ����ת��ΪSO2(g)��SO3(g)����Ӧ���̺�������ϵ������ͼ��ʾ(ͼ�е���H��ʾ����1mol���������)��

��д����ʾS8ȼ�յ��Ȼ�ѧ����ʽ_____________��
��д��SO3�ֽ�����SO2��O2���Ȼ�ѧ����ʽ_________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѡ��2����ѧ�뼼����
����ĺ�ˮ����Լ��1.4��1018t��������������Դ�⡣
��1������ͼ1���ú�ˮ�õ���ˮ�ķ�����___________________________��
��2�����������ǽ��귢չ������һ�ֽϺõĺ�ˮ������������ԭ����ͼ2��ʾ��a�ǵ�Դ��_________���������ų�����__________(���ˮ����Ũˮ��)��
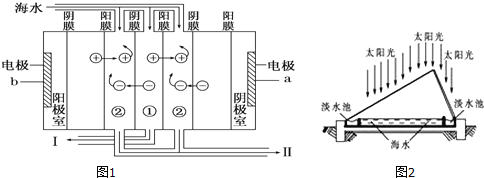
��3����ˮ�������Ũˮ�к������η�(��Ҫ����Mg2+��Ca2+��Fe3+��SO42-)������ˮ�л�ı�ˮ�ʣ��ŵ������лᵼ�������μ���ʲ���ֱ���ŷţ��������ȼҵ���������ǰ��Ҫ��Ũˮ���ƣ������Լ���Ҫ������HCl��NaOH��BaCl2��Na2CO3��)������HCl��������Ҫ��__________________________��
��4�����Ǻ˷�Ӧ����Ҫ��ȼ�ϣ�����������ֱ�ӹ�ϵ��һ�����Һ˹�ҵ��������ķ�չˮƽ����ˮ������UCl4��ʽ����(��������ʽ����)��ÿ�ֺ�ˮֻ��3.3�����ˣ���ˮ���������������൱���ٹ�������̽����ˮ���˵ķ��������ڣ��Ѿ����Ƴɹ�һ�����������ӽ�����֬����ר��������ˮ�е��ˣ�������������Ԫ�أ��䷴Ӧԭ��Ϊ_______________________ (��֬��HR����)���������ӽ���������ӽ���Ĥ���ᴦ�������������õ����˵���Һ���䷴Ӧԭ��Ϊ_________________________��
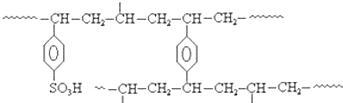
��5�����ӽ�����֬�����Ʊ���ˮ(ȥ����ˮ)����Ҫ������ij�����ӽ��������ľֲ��ṹ��д��(��ͼ)���������ӽ�����֬���ɵ��屽��ϩ�ͽ������Զ���ϩ�����ۺϺ��پ�_____________��Ӧ�õ��ģ�����ˮ������ӽ�����֬�������ú���____________(����ԡ��������ԡ������ԡ�)��
��6���й���������ˮ���������й涨��ˮ����Ӳ�Ȳ��ܹ������Ӳ�ȹ������ú�����彡�����ճ�������һ��Ӱ�죮��ʱӲˮ��Ӳ������__________(�������ӷ���)����ģ���___________(���������)��ɱ�ȥ��������Ӳˮ��Ӳ�ȿ������ӽ�����ȥ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ϊ����ѧ�����ѡ��1����ѡ���⣬
��һ����������Ѽ������������������Ѽ�ײ͵IJ���ԭ�����£��� Ѽ�⡢�� ��ۡ��� �ƹϡ��� ʳ�Ρ���ش�
��1���������۵��� ������ţ���ͬ������2�����������ʵ��� ��
��3������ά���ص��� �� ��4�����ڵ�ζ������ ��
��������������������������ͷ�չ����Ҫ���ʻ�����
��1���Թܡ��ձ�����ƿ�Ȼ�ѧ��������Ҫ������ ��
A������ B���մ�
��2��������Ŀǰ�����������Ͻ𡣸����Ӵ���ˮ�����绯ѧ��ʴ���为����ӦʽΪ ��
A��O2+2H2O + 4e- = 4OH- B��Fe - 2e -= Fe2+
������������ˮ��Ҫ��Դ���ȼҵ�����Ϲ�ҵ��δ�����������ŷš�ij�������Է�ˮ����Ҫ��Hg2+��H+��Na+��Cl���ȣ��Ĵ���������������ͼ��ʾ��
 ��ش�
��ش�
��1��������ˮδ������ֱ���ŷŵ�Σ���� ������ĸ����
a. ���ˮ����Ⱦ b. ���������ж�
��2�����ڷ�ˮpHʱ�������ҺA������ ������ĸ����
a. ���� b. NaOH��Һ
��3��Na2S��Hg2+������Ӧ�����ӷ���ʽ�� ��
��4���÷�ˮ����������й��������£��������Ӻ��Բ��ƣ���
���� | Na+ | Fe2+ | Cl�� | SO42�� |
Ũ�ȣ�mol/L�� | 3.0��10-4 | 2.0��10-4 | 2.5��10-4 |
��c(Fe2+) = mol/L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ۺ�����CO2��CO�Թ�����̼�������Ҫ���塣
��1�� Li4SiO4�����ڸ����õ���Ũ��CO2��ԭ���ǣ���500�棬��Ũ��CO2��Li4SiO4�Ӵ�������������Σ�ƽ��������700�棬��Ӧ������У��ų���Ũ��CO2��Li4SiO4������700��ʱ��Ӧ�Ļ�ѧ����ʽΪ_________________________________��
��2�� �������������(SOEC)���ڸ��µ��CO2��H2O���ȿɸ�Ч�Ʊ��ϳ���(CO��H2)���ֿ�ʵ��CO2�ļ��ţ��乤��ԭ������ͼ��
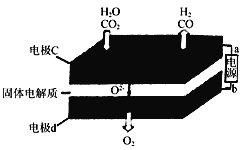
�� bΪ��Դ��________(�������������)��
�� д���缫c�����ĵ缫��Ӧʽ�� __________ ______�� __________________ ______��
��3��������ɵĺϳ����ڴ��������·������·�Ӧ��CO(g)��2H2(g) ![]() CH3OH(g)���Դ˷�Ӧ���������о���
CH3OH(g)���Դ˷�Ӧ���������о���
ij�¶�����һ��ѹ�����зֱ����1.2 mol CO��1 mol H2���ﵽƽ��ʱ�������Ϊ2 L���Һ���0.4 mol CH3OH(g)����÷�Ӧƽ�ⳣ��ֵΪ________����ʱ����������ͨ��0.35 mol CO���壬���ƽ�⽫________(�������Ӧ�������������淴Ӧ����)�ƶ���
��4�� ��֪��

���״���ȼ����Ϊ��H3�����æ�H1����H2����H3��ʾCO(g)��2H2(g) ![]() CH3OH(l)�Ħ�H��
CH3OH(l)�Ħ�H��
��H��______ ____��
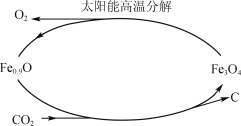
��5������̫���ܺ�ȱ��������[��Fe0.9O]�ɽ�����CO2�Ƚ�Ϊ̼��������ʵ��CO2����Դ����ת�� ��������ͼ��ʾ������1 molȱ��������[Fe0.9O]������CO2��ȫ��Ӧ������________mol C(̼)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2010�괺��2013���������귢��������ʡ�����غ���ǣ����ȫ��������ģ��������Ƕ�ˮ��Դ���ٴ����ӡ�ˮ��������������Ҫ��ѧ���ʣ��й�ˮ�ķ�Ӧ�кܶࡣ
��1���õ���ʽ��ʾH2O���γɹ��� ��
��2����pH=1��ˮ��Һ�У���NH4+��Al3+��Br-��SO42- �� Na+��Fe2+��Cl-��NO3-
��K+��Ba2+��Cl-��NO3- ��K+��Na+��HCO3-��SO42-���������У�һ������������� (�����)��
��3�������з�Ӧ�У�ˮ�������������� (����ĸ����ͬ)��ˮ�Ȳ����������ֲ�����ԭ������ ��
A��2F2��2H2O��4HF��O2 B��2Na2O2��2H2O��4NaOH��O2��
C��CaH2��2H2O��Ca(OH)2��2H2�� D��3Fe��4H2O![]() Fe3O4��4H2]
Fe3O4��4H2]
��4���������ߺš��ɴ��ϵ�������Ҫ������̫���ܺ�ȼ�ϵ�أ�H2��O2��KOH��ˮ��Һ���γ�����ȼ�ϵ�أ������ĵ缫��ӦΪ ����Ӧ������ˮ�����������Ϊ����Ա������ˮ�����õ�1.8 L����ˮʱ�������ת�Ƶĵ�����ԼΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ����̼��һ����;�㷺�Ļ�������ԭ�ϡ��л�����ⷴӦ�����dz��õĴ�������H2��һ�㺬����CO��ʹ�������ж�������Ӧ����������CO������������Ͷ������SO2��ΪŪ��÷����Դ�����Ӱ�죬����������£�
�ش��������⣺
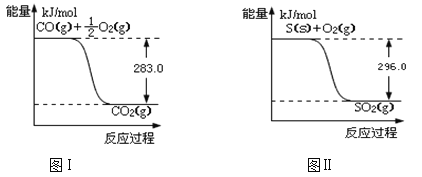
��1��SO2(g) + 2CO(g) ![]() S(s) + 2CO2(g) ��H �� ���÷�Ӧ��ƽ�ⳣ���ı���ʽ�� ��
S(s) + 2CO2(g) ��H �� ���÷�Ӧ��ƽ�ⳣ���ı���ʽ�� ��
��2����ҵ����һ����̼��ȡ�����ķ�ӦΪ��CO(g)+H2O(g) ![]() CO2(g)+H2(g)����֪420��ʱ���÷�Ӧ�Ļ�ѧƽ�ⳣ��K=9�������Ӧ��ʼʱ����2L���ܱ������г���CO��H2O�����ʵ�������0.60mol��5minĩ�ﵽƽ�⣬���ʱCO��ת����Ϊ ��H2��ƽ����������Ϊ mol��L-1��min-1��
CO2(g)+H2(g)����֪420��ʱ���÷�Ӧ�Ļ�ѧƽ�ⳣ��K=9�������Ӧ��ʼʱ����2L���ܱ������г���CO��H2O�����ʵ�������0.60mol��5minĩ�ﵽƽ�⣬���ʱCO��ת����Ϊ ��H2��ƽ����������Ϊ mol��L-1��min-1��
��3��Ϊ�������������ʹ������к����庬�����о�������β����CO��NO��CxHy���ŷ��������ش�����β����Ⱦ��ĺ������/ȼ��(������ȼ�����������)�ı仯��ϵ��ͼ��ʾ��

��֪��N2��O2����NO�ķ�Ӧ�����ȷ�Ӧ������ͣ�
�����/ȼ������CO��CxHy�ĺ������ٵ�ԭ���� ��
������/ȼ�ȴﵽ15��NO���ٵ�ԭ������� ��
��4��һ��������H2��CO�ϳ�CH3OH��CH3OH��ת����ΪCH3OCH3��ת�����Ȼ�ѧ��Ӧ����ʽ���£�2CH3OH(g) ![]() CH3OCH3(g)+H2O(g) ��H=-24.5 kJ��mol-1
CH3OCH3(g)+H2O(g) ��H=-24.5 kJ��mol-1
��250����ѹǿ������ܱ������У�����2mol��CH3OH��һ��ʱ���������Ӧ��ƽ�⣬��ϵ�ų�����11 kJ����ͬһ�����¼���0.2mol CH3OCH3��0.2mol H2O��һ��ʱ���������Ӧ��ƽ�⣬��ϵ����ЧӦΪ .
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��

��1��������A(C4H10O)��һ���л��ܼ���A���Է������±仯��
��A�����еĹ�����������____________��
��Aֻ��һ��һ��ȡ����B��д��A�Ľṹ��ʽ��____________��
��A��ͬ���칹��FҲ�����п�ͼ��A�ĸ��ֱ仯����F��һ��ȡ���������֣�F�Ľṹ��ʽ��
______________________________________��
��2�������HQ��(C6H6O2)��������Ӱ������HQ�����������Ȼ�����Һ������ɫ��Ӧ����HQ�����ܷ����ķ�Ӧ��(ѡ�����)____________________��
�ټӳɷ�Ӧ����������Ӧ���ۼӾ۷�Ӧ����ˮ�ⷴӦ[
��HQ����һ����ȡ����ֻ��һ�֡���HQ���Ľṹ��ʽ��______________________��
��3��A�롰HQ����һ��������������γ�ˮ��һ��ʳƷ����������TBHQ������TBHQ��������������Һ���õõ�����ʽΪC10H12O2Na2�Ļ������TBHQ���Ľṹ��ʽ��____________________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com