
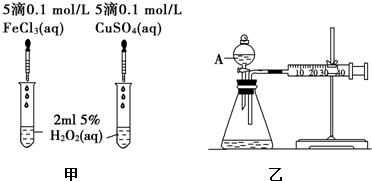
分析 (1)根据反应生成气体的快慢分析来比较催化效果;根据H2O2分解的催化作用有可能是氯离子起的作用,改为Fe2(SO4)3使阳离子相同,更为合理;根据反应物、生成物、反应条件写出反应方程式;
(2)A为分液漏斗,根据乙图装置来选择气密性的检查方法;该反应是通过反应速率分析的,所以根据v=$\frac{△c}{△t}$来判断.
解答 解:(1)根据反应生成气体的快慢分析来比较催化效果;在探究Fe3+和Cu2+对H2O2分解的催化效果是,必须保持其他的条件相同,所以将FeCl3改为Fe2(SO4)3更为合理,可以避免由于阴离子不同造成的干扰,过氧化氢分解生成水和氧气,反应方程式为:2H2O2$\frac{\underline{\;MnO_{2}\;}}{\;}$2H2O+O2↑,
故答案为:反应产生气泡的快慢;可以排除阴离子不同对实验的干扰;2H2O2$\frac{\underline{\;MnO_{2}\;}}{\;}$2H2O+O2↑;
(2)由图可知,A为分液漏斗;气密性的检查方法是关闭分液漏斗活塞,将注射器活塞向外拉出一段,过一会后看其是否回到原位;定量比较Fe3+和Cu2+对H2O2分解的催化效果,可以通过测定产生40mL的气体所需的时间来比较,产生40mL的气体所需的时间越短,则催化效果越好,
故答案为:分液漏斗;关闭分液漏斗活塞,将注射器活塞向外拉出一段,过一会后看其是否回到原位;收集40 mL气体所需要的时间.
点评 本题主要考查了催化剂的作用及化学反应速率的影响因素等知识点,难度不大,要会分析将FeCl3改为Fe2(SO4)3更为合理的理由.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题

| A. | c(NH+4)相等的①NH4Cl②(NH4)2SO4③NH4HSO4溶液中,pH大小:①>②>③ | |
| B. | 0.1mol/LNa2S溶液:c(OH-)=c(H+)+c(HS-)+c(H2S) | |
| C. | 25℃时,pH=2的CH3COOH与pH=12的NaOH溶液等体积混合:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) | |
| D. | 已知酸性HF>CH3COOH,pH相等的NaF与CH3COOK溶液中:[c(Na+)-c(F-)]<[c(K+)-c(CH3COO-)] |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X2Y3 | B. | XY3 | C. | X2Y2 | D. | X3Y2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 品名:XX火腿肠 净含量:150g 生产日期:见封口 保质期:25℃以下6个月 配料:精选瘦肉、大豆蛋白、鸡蛋、淀粉、白砂糖、食盐、 食用香精、山梨酸钾、亚硝酸钠、维生素C 储存指南:避免日晒,置阴凉干燥处 生产厂家:XX食品有限公司 地址:XX市XX路XX号 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
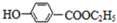 ,下列反应①-⑥是其合成过程,其中某些反应条件及部分反应物或生成物未注明.
,下列反应①-⑥是其合成过程,其中某些反应条件及部分反应物或生成物未注明.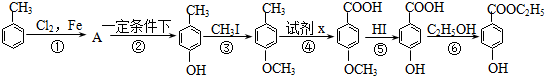 ).
).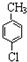 .A的名称为对氯甲苯.
.A的名称为对氯甲苯.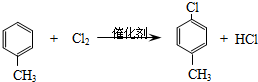 .
.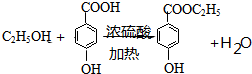 .
. 的同分异构体中,既能与NaHCO3发生反应,又能与FeCl3溶液发生显色反应的共有13种,其中核磁共振氢谱为5组峰,且峰面积比为2:2:2:1:1的为
的同分异构体中,既能与NaHCO3发生反应,又能与FeCl3溶液发生显色反应的共有13种,其中核磁共振氢谱为5组峰,且峰面积比为2:2:2:1:1的为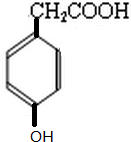 (写结构简式).
(写结构简式).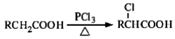 ,写出以苯酚和乙醇为原料制备
,写出以苯酚和乙醇为原料制备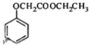 的合成路线流程图(无机试剂任用).合成路线流程图例如下:
的合成路线流程图(无机试剂任用).合成路线流程图例如下:查看答案和解析>>
科目:高中化学 来源: 题型:实验题
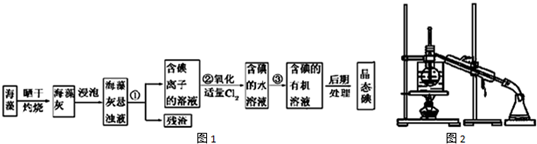
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同主族金属原子半径的大小 | |
| B. | 单质的熔沸点高低 | |
| C. | 与酸反应的剧烈程度 | |
| D. | 最高价氧化物对应水化物的碱性强弱 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com