
 NO������⻯ѧ�������ƻ������㣮����NO�ж��ַ��������������ش��������⣺
NO������⻯ѧ�������ƻ������㣮����NO�ж��ַ��������������ش��������⣺| ʱ�䣨s�� | 0 | 1 | 2 | 3 | 4 | �� |
| c��NO��/mol•L-1 | 1.00��10-3 | 4.00��10-4 | 1.70��10-4 | 1.00��10-4 | 1.00��10-4 | �� |
���� ��1�����ݱ������������ǰ2s�ڵ�ƽ����Ӧ���ʦԣ�NO��=��1.00��10-3-1.70��10-4 ����2=4.15��10-4mol/��L•s�������ݻ�ѧ��Ӧ����֮�ȵ��ڻ�ѧ������֮�ȣ��ԣ�N2��=1/2�ԣ�NO��=2.08��10-4 mol/��L•s�����ɱ������ݿ�����3s��c��NO���������ƽ�⣬��ʱc��CO��=1.00��10-4mol•L-1��c��CO2��=1.00��10-3mol•L-1 -1.00��10-4mol•L-1=9.00��10-4mol•L-1��c��N2��=1/2c��CO2��=4.50��10-4mol•L-1������K=c��CO2��2��c��N2��/��c��NO��2��c��CO��2��=3.65��106��
��2���ﵽƽ��ʱ��Ҫ���NOת���ʣ����ı�����Ҫʹƽ�������ƶ���
A��ѡ�ø���Ч�Ĵ�����ƽ�ⲻ�ƶ�����A����
B�����ͷ�Ӧ��ϵ���¶ȣ��÷�ӦΪ���ȷ�Ӧ�������ƶ�����B��ȷ��
C���������ʹ������ѹǿ����ƽ�ⲻ�ƶ�����C����
D������COʹ������ѹǿ�����൱������COŨ�ȣ�ƽ�������ƶ���NOת������ߣ���D��ȷ��
��3������֪���̢�2NO��g��+2CO��g��=2CO2��g��+N2��g����H=-748kJ/mol����N2��g��+O2��g��=2NO��g����H=+180kJ/mol�����ݸ�˹���ɢ١�2+�ڡ�2��CO��ȼ���ȵ��Ȼ�ѧ����ʽΪCO��g��+1/2O2��g��=CO2��g����H=��-748kJ/mol����2+��+180kJ/mol����2=-284 kJ/mol��
��4��O3����NO���ˮϴ�ɲ���HNO3��O2��ת�Ƶ�����=���ϼ���������NOת��ΪHNO3 �����ϼ�����3��ÿ����1mol��HNO3ת��3mol����
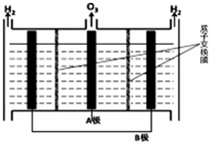
��5��������֪ͼ��A����������O3��B����������H2��˵��A��������������ӦΪ������B��������ԭ��ӦΪ���������������Ե缫���ĵ缫��ӦʽΪ3H2O-6e-=O3+6H+
��� �⣺��1�����ݱ������������ǰ2s�ڵ�ƽ����Ӧ���ʦԣ�NO��=��1.00��10-3-1.70��10-4 ����2=4.15��10-4mol/��L•s�������ݻ�ѧ��Ӧ����֮�ȵ��ڻ�ѧ������֮�ȣ��ԣ�N2��=1/2�ԣ�NO��=2.08��10-4 mol/��L•s�����ɱ������ݿ�����3s��c��NO���������ƽ�⣬��ʱc��CO��=1.00��10-4mol•L-1��c��CO2��=1.00��10-3mol•L-1 -1.00��10-4mol•L-1=9.00��10-4mol•L-1��c��N2��=1/2c��CO2��=4.50��10-4mol•L-1������K=c��CO2��2��c��N2��/��c��NO��2��c��CO��2��=3.65��106��
�ʴ�Ϊ��2.08��10-4 mol/��L•s����3.65��106��
��2���ﵽƽ��ʱ��Ҫ���NOת���ʣ����ı�����Ҫʹƽ�������ƶ���
A��ѡ�ø���Ч�Ĵ�����ƽ�ⲻ�ƶ�����A����
B�����ͷ�Ӧ��ϵ���¶ȣ��÷�ӦΪ���ȷ�Ӧ�������ƶ�����B��ȷ��
C���������ʹ������ѹǿ����ƽ�ⲻ�ƶ�����C����
D������COʹ������ѹǿ�����൱������COŨ�ȣ�ƽ�������ƶ���NOת������ߣ���D��ȷ��
�ʴ�Ϊ��BD��
��3������֪���̢�2NO��g��+2CO��g��=2CO2��g��+N2��g����H=-748kJ/mol��
��N2��g��+O2��g��=2NO��g����H=+180kJ/mol��
���ݸ�˹���ɣ���+�ڣ���$\frac{1}{2}$��CO��ȼ���ȵ��Ȼ�ѧ����ʽΪ��CO��g��+$\frac{1}{2}$O2��g��=CO2��g����H=��-748kJ/mol����$\frac{1}{2}$+��+180kJ/mol����$\frac{1}{2}$=-284 kJ/mol��
�ʴ�Ϊ��CO��g��+$\frac{1}{2}$O2��g��=CO2��g����H=-284 kJ/mol��
��4��O3����NO���ˮϴ�ɲ���HNO3��O2��ת�Ƶ�����=���ϼ���������NOת��ΪHNO3 �����ϼ�����3��ÿ����1mol��HNO3ת��3mol���ӣ�
�ʴ�Ϊ��3��
��5��������֪ͼ��A����������O3��B����������H2��˵��A��������������ӦΪ������B��������ԭ��ӦΪ���������������Ե缫���ĵ缫��ӦʽΪ3H2O-6e-=O3+6H+��
�ʴ�Ϊ��B��3H2O-6e-=O3+6H+��
���� ���⿼���˷�Ӧ���ʡ�ƽ�ⳣ����ת���ʵļ��㣬��Ӧ�����仯�ķ����жϺ��Ȼ�ѧ����ʽ����д����ѧƽ���Ӱ�����ط���Ӧ�ã�ƽ�ⳣ�����㣬�缫����ʽ����д�ȣ����ջ����ǽ���ؼ�����Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na��O | B�� | Na+��O2- | C�� | Mg��Na | D�� | ?����2+��Na+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 10��1 | B�� | 100��1 | C�� | 1��100 | D�� | ��ȷ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ?
? ��g��+H2��g����H=+124kJ•mol-1
��g��+H2��g����H=+124kJ•mol-1| ��ѧ�� | C-H | C-C | C=C | H-H |
| ����/kJ•mol-1 | 412 | 348 | x | 436 |
 +Cl2��g��?
+Cl2��g��? +HCl��g����H2��0
+HCl��g����H2��0
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
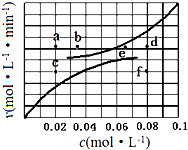 ��1.0L�ܱ������з���0.10molA��g������һ���¶Ƚ������·�Ӧ��
��1.0L�ܱ������з���0.10molA��g������һ���¶Ƚ������·�Ӧ��| ʱ��t/h | 0 | 1 | 2 | 4 | 8 | 16 |
| ��ѹǿp/100kPa | 4.91 | 5.58 | 6.32 | 7.31 | 8.54 | 8.54 |
| c��A��/��mol•L-1�� | 0.10 | 0.086 | 0.071 | 0.051 | a | a |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | m=-26.5��2c=a-b | B�� | m=-53��c2=$\frac{a}{b}$ | C�� | m=-26.5��c2=$\frac{a}{b}$ | D�� | m=-53��2c=a-b |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��2.0mLŨ�Ⱦ�Ϊ0��lmol•L-l��KC1��KI�����Һ�еμ�1��2��0.0lmol/LAgNO3��Һ���������ʻ�ɫ��˵��AgCl��Ksp��Agl��Ksp�� | |
| B�� | ��ϡ�����м���ͭ�ۣ�ͭ�۲��ܽ⣻�ټ���������H2O2��ͭ���Բ��ܽ� | |
| C�� | ��AIC13��Һ�еμӰ�ˮ��������ɫ�������ټ���NaHSO4��Һ����������ʧ | |
| D�� | ��CO2ͨ��Ba��NO3��2��Һ�������ͣ�������������ͨ��SO2��Ҳ�������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com