
(14分)BaS是一种白色晶体,微溶于水,可用于制备立德粉、Na2S等。工业上可用H2与重晶石(BaSO4)在高温下反应制备BaS,热化学方程式为BaSO4(s)+4H2(g) BaS(s)+4H2O(g)
BaS(s)+4H2O(g)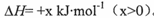 。回答下列问题:
。回答下列问题:
(1)在温度和容积不变的条件下,能说明该反应己达到平衡状态的是 (填字母序号)。
a.n(H2)=n(H2O)
b.容器内压强保持不变
c.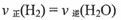
d.水蒸气的浓度保持不变
(2)平衡后下列措施既可提高反应速率,又可提高H2的转化率的是 (填字母序号)。
a.使用催化剂
b.升高反应体系的温度
c.增大反应容器的体积
d.及时从反应体系中分离出水蒸气
(3)将温度恒定为T℃,向体积为2L的密闭容器中加入一定量的重晶石和H2。在不同时间测得H2的物质的量如下表:

①2t时,n 1.20(填“>”、“<”或“=”)
②若氢气的平衡转化率为a,则该温度下反应的化学平衡常数K= (用含a的
代数式表示);若测得该反应达到平衡时吸热Q kJ ,则x= (用含a、Q的代数式表示)。
(4)为了探究温度、固体反应物的表面积对化学反应速率的影响,某同学在一固定容积的密闭容器中加入一定量的重晶石和H2,设计了下表中的三组实验:
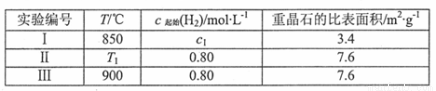
①填写上表中的实验条件: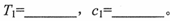
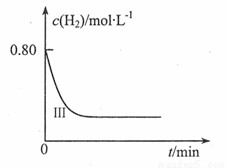
②在直角坐标系中画出I, II两组实验氢气的浓度随时间变化趋势图,并在每条曲线上标明对应的实验编号。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2014-2015学年江苏省泰州市高三第二次模拟考试化学试卷(解析版) 题型:选择题
下列有关物质的性质与应用对应关系不正确的是
A.常温下铁与浓硝酸发生钝化,常用铁罐车运输浓硝酸
B.SO2有漂白性,常用来漂白纸浆
C.硅酸钠溶液呈碱性,常用作木材的防火剂
D.Al具有良好延展性和抗腐蚀性,常用铝箔包装物品
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省益阳市高三四月调研考试理综化学试卷(解析版) 题型:填空题
【化学——选修2:化学与技术】(15分)氮的化合物是重要的化工原料,在工农业生产中有很多重要应用。工业上合成氨的流程示意图如下:
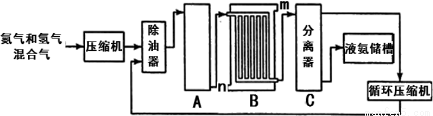
回答下列问题:
(1)25℃时合成氨反应热化学方程式为:N2(g)+3H2(g) 2NH3(g) ΔH=-92.4 kJ/mol。在该温度时,取1 mol N2和3 mol H2放在密闭容器中,在催化剂存在下进行反应,测得反应放出的热量总是小于92.4 kJ。其原因是______________。
2NH3(g) ΔH=-92.4 kJ/mol。在该温度时,取1 mol N2和3 mol H2放在密闭容器中,在催化剂存在下进行反应,测得反应放出的热量总是小于92.4 kJ。其原因是______________。
(2)原料氢气的来源是水和碳氢化合物,写出工业生产中分别采用煤和天然气为原料制取氢气的化学反应方程式: , 。
(3)设备B的名称是________,其中m和n是两个通水口,入水口是 (填“m”或“n”),不宜从相反方向通水的原因 。
(4)设备C的作用是 。
(5)为了提高其产量,降低能耗,近年有人将电磁场直接加在氮气与氢气反应的容器内,在较低的温度和压强条件下合成氨,获得了较好的产率。从化学反应本质角度分析,电磁场对合成氨反应的作用是 ;与传统的合成氨的方法比较,该方法的优点是 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省怀化市高三第二次模拟考试理综化学试卷(解析版) 题型:选择题
下列溶液中微粒的关系不正确的是
A.已知A— + H2B(过量)= HA + HB—,则结合H+的能力:HB—<A—<B2—
B.在25℃时,将cmol/L的醋酸溶液与0.02mol/LNaOH溶液等体积混合后溶液恰好呈中性,用含c的代数式表示CH3COOH的电离常数Ka=2×10-9/(c-0.02)
C.若将CO2 通入0.1 mol/LNaOH溶液中至溶液中性,则溶液中2 c(CO32ˉ)+ c(HCO3ˉ)= 0.1 mol/L
D.常温下,将相同体积的pH=3硫酸和pH=11一元碱BOH溶液混合,所得溶液可能为中性也可能为碱性
查看答案和解析>>
科目:高中化学 来源:2014-2015学年云南省毕业生复习统一检测理综化学试卷(解析版) 题型:推断题
【化学—选修5:有机化学基础】(15分)酚醛树脂是一种合成塑料。线型酚醛树脂可通过如下路线合成:
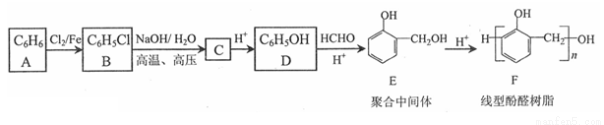
回答下列问题:
(1)B的官能团为 ,C的化学式为
(2)A生成B的化学方程式为 ,反应类型为
(3)D生成E的反应类型是 ,若D与HCHO按物质的量1:3发生类似反应,则生成另一种聚合中间体的结构简式为
(4)E的同分异构体中,属于二元酚的共有 种,其中核磁共振氢谱有四组吸收峰,且峰面积比为3:2:2:1的是 (写出其中一种的结构简式)o
(5)尿素[CO(NH2)2〕分子中氮原子上的氢原子可以像苯环上的氢原子那样与甲醛发生类似D→E→F的反应,则生成线型脉醛树脂的结构简式为
查看答案和解析>>
科目:高中化学 来源:2014-2015学年云南省毕业生复习统一检测理综化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值,下列说法正确的是
A.4gNaOH固体所含电子总数为2NA
B.22.4LC2H6所含化学键总数为7 NA
C.常温常压下,14gCO、N2混合气体所含分子总数为NA
D.0.1 mol-1LNH4C1溶液中,NH4+与Cl一数之和小于0.2 NA
查看答案和解析>>
科目:高中化学 来源:2014-2015学年天津市七校高三4月联考化学试卷(解析版) 题型:选择题
某密闭容器中充入等物质的量的A和B,一定温度下发生反应A(g)+xB(g) 2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化如下图所示。下列说法中正确的是
2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化如下图所示。下列说法中正确的是

A.30min时降低温度,40min时升高温度
B.反应方程式中的x=1,正反应为吸热反应
C.8min前A的平均反应速率为0.08mol/(Lmin)
D.30min~40min间该反应使用了催化剂
查看答案和解析>>
科目:高中化学 来源:2014-2015学年天津市和平区高三第二次模拟考试理综化学试卷(解析版) 题型:推断题
(18分)已知:

香豆素的主要成分是芳香内酯A,A经下列步骤转化为水杨酸。
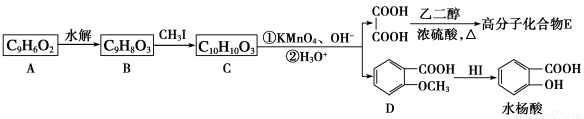
请回答下列问题:
(1)写出A的结构简式_______________________。
(2)B分子中有2个含氧官能团,分别为____和___(填官能团名称),B→C的反应类型为_________。
(3)在上述转化过程中,反应步骤B→C的目的是___________________________。
(4)下列有关A、B、C的叙述中不正确的是________(填序号)。
a.C的核磁共振氢谱中共有8组峰
b.A、B、C均可发生加聚反应
c.1 mol A最多能与5 mol氢气发生加成反应
d.B能与浓溴水发生取代反应
(5)化合物D有多种同分异构体,其中一类同分异构体是苯的对二取代物,且水解后生成的产物之一能发生银镜反应,请写出其中一种的结构简式:_______________。
(6)写出合成高分子化合物E的化学反应方程式:___________________________。
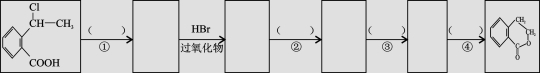
(7)写出以 为原料制
为原料制 的合成路线流程图(无机试剂任用),在方框中填出相应的物质,并在括号注明反应条件。合成路线流程图示例如下:
的合成路线流程图(无机试剂任用),在方框中填出相应的物质,并在括号注明反应条件。合成路线流程图示例如下:
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市闵行区高三下学期质量调研考试(二模)化学试卷(解析版) 题型:计算题
(本题共14分)工业上用氨气与空气混合,通过“氨的催化氧化”等反应工业合成硝酸及其他产品。
1.将NH3与O2在一定条件下充分反应后全部转化为硝酸溶液,则此硝酸溶液中溶质的质量分数为_________________,若所得硝酸密度为ρg/cm3,则其物质的量浓度为 (保留两位小数)。
2.某化肥厂以氨为原料制备 NH4NO3,已知由氨制 NO 的产率是 96%,NO 制硝酸的产率是 92%,氨被硝酸的吸收率为100%,则制备80吨 NH4NO3所需氨的体积(标准状况)为 m3(保留两位小数)。
3.一定量的浓硝酸与铜反应生成NO、NO2、N2O4混合气体。测出混合气体密度是同温同压下氢气的28倍。再将气体通过足量水充分吸收后,体积变为原来的2/3(相同条件下测定)。计算混合气体中NO2的体积分数。
4.合成氨原料气由CH4在高温下与水蒸气、空气反应而得。反应原理如下:
CH4+2H2O→CO2+4H2 2CH4+O2+2H2O→2CO2+6H2
将反应后的混合气中CO2、H2O (g)通过吸收和干燥除去后,只含N2和H2。为使进入合成氨反应塔两者体积比为1∶3。计算起始气体中CH4和空气的比例。(已知空气中O2和N2的体积比为1∶4)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com