
����Ŀ����һ�����İ�������粒����������Ƶ��ܱ���������У�����������䣬��������������Բ��ƣ���ʹ��ﵽ�ֽ�ƽ�⣺NH2COONH4(s)![]() 2NH3(g)��CO2(g)��ʵ���ò�ͬ�¶��µIJ���ƽ���������±���
2NH3(g)��CO2(g)��ʵ���ò�ͬ�¶��µIJ���ƽ���������±���
�¶�/�� | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
ƽ����ѹǿ/kPa | 5.7 | p1 | 12.0 | p2 | 24.0 |
ƽ��������Ũ��/10��3 mol��L��1 | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
����˵���в���ȷ����
A. ��������ƽ����Է�����������M������ʱ��仯ʱ��Ӧ��ƽ��״̬
B. 15.0 ��ʱNH2COONH4(s)�ֽ��ƽ�ⳣ��Ϊ2.0��10��9(mol/L)3
C. �÷�ӦH��0��p2��2p1
D. ���ں����½�ƽ����ϵ������룬�ٴ�ƽ���c(NH3)��c(CO2)����ԭƽ���
���𰸡�A
������������A��ֻ�в��������壬�ʷ�Ӧ�����л�������ƽ����Է�����������M����ʱ��仯���ʲ�����ʱ��仯ʱ��Ӧ��ƽ��״̬��A�����B���轫15 ������Ũ��ת��ΪNH3��CO2��Ũ�ȣ�
c��NH3����![]() ��2.4��10��3mol��L��1��1.6��10��3mol��L��1��c��CO2����
��2.4��10��3mol��L��1��1.6��10��3mol��L��1��c��CO2����![]() ��2.4��10��3mol��L��1��0.8��10��3mol��L��1��K����1.6��10��3��2��0.8��10��3��0.2��10��8��B����ȷ��C���¶�����K����Ϊ���ȷ�Ӧ��ƽ����Ũ�Ⱥ�����ǰ�ߵ���������p2��2p1��C����ȷ��D�����ں����½�ƽ����ϵ������룬ƽ��������ƶ������ٴ�ƽ���c(NH3)��c(CO2)����ԭƽ���D����ȷ����ѡA��
��2.4��10��3mol��L��1��0.8��10��3mol��L��1��K����1.6��10��3��2��0.8��10��3��0.2��10��8��B����ȷ��C���¶�����K����Ϊ���ȷ�Ӧ��ƽ����Ũ�Ⱥ�����ǰ�ߵ���������p2��2p1��C����ȷ��D�����ں����½�ƽ����ϵ������룬ƽ��������ƶ������ٴ�ƽ���c(NH3)��c(CO2)����ԭƽ���D����ȷ����ѡA��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����»���Ϊa kJ��mol-1����ѧ��Ϊb kJ��mol-1�����Ϊc kJ��mol-1����a��b��c�Ĵ�С��ϵ��ȷ����
A. a��b��cB. b��a��cC. c��b��aD. b��c��a
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪A��һ����̬������ȫȼ��ʱ������ˮ�Ͷ�����̼�����ʵ���֮��Ϊ1��1��A����Է�������С��30������ͼ�仯�У��м����C�ܺ����Ƶ�������ͭ��Ӧ����ש��ɫ����������Ӧ����δд����
��֪2CH3CHO+O2![]() 2CH3COOH����ش��������⣺
2CH3COOH����ش��������⣺
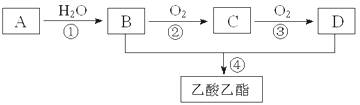
��1��д��A�ĵ���ʽ________
��2��B��D�����ں��еĹ����ŷֱ���________��________�������ƣ���
��3���ж����з�Ӧ�ķ�Ӧ���ͣ���______________����______________
��4��д�����з�Ӧ�Ļ�ѧ����ʽ����________________________________________��
��5������˵����ȷ����________��
A���л���B������Ʒ�Ӧ���������Ƹ���Һ�棬��ͣ���ζ��������ʧ��
B���л���B��D�Լ������������ñ���Na2CO3��Һ����
C����Ӧ���У�Ũ������Ҫ����������
D���л���C�ܱ����Ƽ���������ͭ����Һ������KMnO4��Һ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ģ�CO��NO2������β������Ҫ��Ⱦ�����β���ķ�Ӧʽ֮һΪ��2NO��g��+2CO��g���TN2��g��+2CO2��g������ش��������⣺
��1����֪��N2��g��+O2��g���T2NO��g����H=+180.5kJ/mol
C��s��+O2��g���TCO2��g����H=��393.5kJ/mol
2C��s��+O2�T2CO��g����H=��221kJ/mol
��2NO��g��+2CO��g���TN2��g��+2CO2��g����H=______��
��2��һ���¶��£���һ���ΪVL���ܱ������г���һ������NO��COʱ����Ӧ���е�tʱ��ʱ�ﵽƽ��״̬����ʱn��CO��=a mol��n��NO��=2a mol��n��N2��=b mol����N2ռƽ���������ܼ������1/4��
���÷�Ӧ��ƽ�ⳣ��K=______����ֻ��a��V��ʽ�ӱ�ʾ��
���жϸ÷�Ӧ�ﵽƽ��ı�־��______������ţ�
A��v��CO2������=v��CO������
B����������ƽ����Է����������ٸı�
C�����������ܶȲ��ٸı�
D��NO��CO��N2��CO2�����ʵ���Ũ�Ⱦ����ٱ仯
��3����һ���¶��£���2.0mol NO��2.4mol COͨ��̶��ݻ�2L���ܱ������У���Ӧ�����в������ʵ����ʵ����仯��ͼһ��ʾ��

�����к�����NO��ת������______��0��15min CO2��ƽ����Ӧ����v��CO2��=______��20minʱ�����ı䷴Ӧ����������COŨ�ȼ�С����ı��������______������ţ�
A������CO2���� B��������� C�������¶� D�������ݻ����
��4��ͨ��NOX�������ɼ��NOX�ĺ������乤��ԭ����ͼ����ʾ��
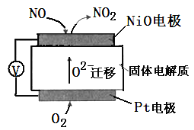
����Pt�缫�Ϸ�������______��Ӧ������������������ԭ������NiO�缫�ϵĵ缫��ӦʽΪ______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ����ij�������Na2A��Һ��ͨ��HCl,��Һ��-lg![]() ��-lgc(HA-)��-lg
��-lgc(HA-)��-lg![]() ��-1gc(A2-)�Ĺ�ϵ��ͼ��ʾ������˵����ȷ���ǣ� ��
��-1gc(A2-)�Ĺ�ϵ��ͼ��ʾ������˵����ȷ���ǣ� ��
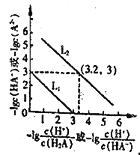
A. ֱ��L2��ʾ-lg![]() ��-lgc(HA-)�Ĺ�ϵ
��-lgc(HA-)�Ĺ�ϵ
B. ͨ��HCl�����У�ˮ�����c(OH-)��ˮ�����c(H+)�ij˻���������
C. c(H2A)��������Ϊ10-7
D. ��NaHA��Һ��c(Na+)>(HA-)>c(H2A)>c(A2-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ��ʾװ�ý�������ʵ�飬ʵ������Ԥ�������һ�µ���
���е����� | ���е����� | Ԥ���������� | |
A | ���۵⻯����Һ | Ũ���� | ���������� |
B | ��̪��Һ | Ũ���� | ���������� |
C | �Ȼ�����Һ | Ũ��ˮ | �а�ɫ���� |
D | ʪ���ֽ�� | ������ˮ | ��ֽ����ɫ |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����12CO��14CO��ɵĻ������Ժ���������ܶ�Ϊ7.125������������12C��14C��ԭ�Ӹ�����Ϊ(�� ��)
A. 1��1 B. 1��2 C. 3��1 D. 2��3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�˵����ȷ����
A. ��ͭ����Ʒ�Ʋ������,����Ʒ������ǰ����������
B. �����ʵ���Ũ�ȵ�CH3COOH��Һ��HCl��Һ��,ˮ�ĵ���̶���ͬ
C. 0.1mol/LNa2CO3��Һ:c(OH-)=c(H2CO3)+c(HCO3-)+c(H+)
D. ���ڷ�Ӧ2SO2+O2![]() 2SO3,ʹ�ô����ܼӿ췴Ӧ���ʺ����SO2ƽ��ת����
2SO3,ʹ�ô����ܼӿ췴Ӧ���ʺ����SO2ƽ��ת����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����200 ��ʱ����a mol H2(g)��b mol I2(g)���뵽���ΪV L���ܱ����У�������Ӧ��I2(g)��H2(g)![]() 2HI(g)��
2HI(g)��
(1)��Ӧ�տ�ʼʱ������c(H2)��______ mol��L��1����c(HI)��________�����Ի�ѧ��Ӧ����________���(��v(��)��v(��))��
(2)���ŷ�Ӧ�Ľ��У���Ӧ������и����Ũ�ȵı仯����Ϊc(H2)_____����c(HI)_____ ���Ӷ���ѧ��Ӧ����v(��) _______ (���С��������)��
(3)����Ӧ���е�v(��)��v(��)________ʱ���˿��淴Ӧ�ﵽ������ȡ������������������ʱ��������и���ֵ����ʵ��������ʵ���Ũ�ȡ����������������������Ӧ���ת���ʺ�������IJ��ʶ���________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com