
| 选项 | 实验操作与现象 | 结论 |
| A | 向鸡蛋清溶液中滴加醋酸铅溶液,产生白色沉淀,加水沉淀不消失 | 蛋白质发生了变性 |
| B | 测定浓度均为0.1mol•L-1 CH3COONa与HCOONa溶液的pH,CH3COONa溶液的pH较大 | 酸性:CH3COOH>HCOOH |
| C | 苯酚的浊液中加入碳酸钠溶液,溶液变为无色 | 酸性:苯酚>碳酸氢钠溶液 |
| D | 向浓度均为0.1mol•L-1 NaCl和NaI混合溶液中滴加3滴0.1mol•L-1 AgNO3溶液,出现黄色沉淀 | 溶解度:AgI<AgCl |
| A. | A | B. | B | C. | C | D. | D |
分析 A.鸡蛋清溶液中滴加醋酸铅溶液,发生变性,为不可逆过程;
B.等浓度时,盐的水解程度越大,对应酸的酸性越弱;
C.发生强酸制取弱酸的反应;
D.Ksp小的先沉淀.
解答 解:A.鸡蛋清溶液中滴加醋酸铅溶液,发生变性,为不可逆过程,则产生白色沉淀,加水沉淀不消失,故A正确;
B.等浓度时,盐的水解程度越大,对应酸的酸性越弱,由CH3COONa溶液的pH较大可知,酸性:CH3COOH<HCOOH,故B错误;
C.发生强酸制取弱酸的反应,由苯酚的浊液中加入碳酸钠溶液,溶液变为无色,可知酸性:苯酚>碳酸氢钠溶液,故C正确;
D.Ksp小的先沉淀,由出现黄色沉淀,可知溶解度:AgI<AgCl,故D正确;
故选B.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质、酸性比较、沉淀生成、实验技能为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | SiO2$→_{△}^{NaOH(aq)}$Na2SiO3$\stackrel{CO_{2}}{→}$H2SiO3 | |
| B. | S$→_{点燃}^{O_{2}}$SO2$\stackrel{BaCl_{2}(aq)}{→}$BaSO3 | |
| C. | NH3$→_{催化剂/△}^{O_{2}}$NO2$\stackrel{H_{2}O}{→}$HNO3 | |
| D. | MgCl2•6H2O$\stackrel{△}{→}$MgCl2$\stackrel{电解}{→}$Mg |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
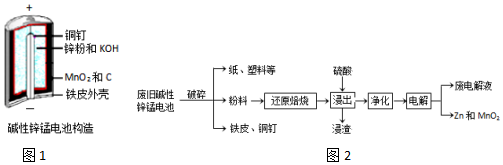
| 化合物 | Mn(OH)2 | Zn(OH)2 | Fe(OH)3 |
| KSP近似值 | 10-13 | 10-17 | 10-38 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 操作 | 目的或结论 |
| A | 将Fe(NO3)2晶体溶于稀硫酸后,滴加KSCN溶液,观察溶液是否变化 | 检验Fe(NO3)2样品是否已被氧化而变质 |
| B | 海带提碘实验中,为了制取海带灰的浸取液,需要煮沸海带灰和水的混合物1-2min | 主要目的是去除溶液中的氧气,避免氧气氧化碘离子 |
| C | 在试管中依次加入2mL浓硫酸、3mL乙醇和2mL乙酸,用酒精灯缓慢加热 | 制备乙酸乙酯 |
| D | 向盛有少量Mg(OH)2固体的试管中加入适量NH4Cl浓溶液,充分震荡,白色固体溶解 | NH4+与Mg(OH)2溶解出的OH-结合,导致Mg(OH)2溶解 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH3分子的电子式: | |
| B. | 次氯酸的结构式:H-Cl-O | |
| C. | CH4分子的结构式: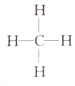 | |
| D. | 用电子式表示氯化氢分子的形成过程: |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | MgSO4与Ba(OH)2溶液反应:SO42-+Ba2+=Ba SO4↓ | |
| B. | CuSO4溶液吸收H2S气体:Cu2++S2-=CuS↓ | |
| C. | AlCl3 溶液中加入过量的浓氨水:Al3++4NH3•H2O=A1O2-+4NH4++2H2O | |
| D. | 等体积、等浓度的Ba(OH)2稀溶液与NH4HCO3稀溶液混合:Ba2++2OH-+NH4++HCO3-=BaCO3↓+NH3•H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 9:4 | B. | 4:9 | C. | 2:1 | D. | 1:2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com