
A、 |
B、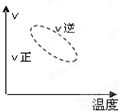 |
C、 |
D、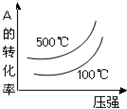 |


科目:高中化学 来源: 题型:
| A、1:2 | B、8:1 |
| C、16:207 | D、71:216 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 2CO2(g)+N2(g)△H<0
2CO2(g)+N2(g)△H<0| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO) (mol/L) |
1.00×10-3 | 4.50×10-4 | 2.50×10-4 | 1.50×10-4 | 1.00×10-4 | 1.00×10-4 |
| c(CO) (mol/L) |
3.60×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
| 实验 编号 |
T(℃) | NO初始浓度 (mol/L) |
CO初始浓度 (mol/L) |
催化剂的比表面积(m2/g) |
| Ⅰ | 280 | 1.20×10-3 | 5.80×10-3 | 82 |
| Ⅱ | 280 | 1.20×10-3 | 5.80×10-3 | 124 |
| Ⅲ | 350 | 1.20×10-3 | 5.80×10-3 | 124 |

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、粗盐提纯时,为了加快过滤速率,可用玻璃棒搅拌过滤器中的液体 |
| B、容量瓶检漏:在容量瓶中注入适量的水,塞上玻璃瓶塞,左手五指托住瓶底,右手食指顶住瓶塞,反复倒置数次,观察是否漏水 |
| C、用分液法分离C2H5OH与H2O的混合物 |
| D、测定溶液pH的操作:将pH试纸置于表面皿上,用玻璃棒蘸取溶液,点在pH试纸的中部,与对应的标准比色卡比较 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 溶液 | 操作及现象 |
| A | CaC12溶液 | 通入CO2,溶液不变浑浊;再通入氨气,溶液变浑浊 |
| B | Na2SiO3溶液 | 通入CO2,溶液变浑浊;继续通CO2至过量,浑浊消失 |
| C | Ca(C1O)2溶液 | 通入CO2,溶液变浑浊;再加入品红溶液,红色不褪去 |
| D | BaC12溶液 | 先通入NO2,再通入SO2至过量,先生成沉淀后沉淀消失 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| B、c(OH-)=c(H+)+c(CH3COOH) |
| C、c(Na+)=c(CH3COO-)+c(CH3COOH) |
| D、c(Na+)+c(H+)=c(CH3COO-)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
 A、B、C、D是中学化学常见的四种物质,它们的转化关系如下:A+B=C+D
A、B、C、D是中学化学常见的四种物质,它们的转化关系如下:A+B=C+D查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com