
分类法是学习化学的重要方法,人们在认识事物时可采用多种分类方法。下表各组归类
| 序号 | 分类标准 | 归类 |
| A | FeSO4、NO2、MnO2、NaClO、Cu3P、Na2O2 | H2SO3 |
| B | CH3COOH、HOOC—COOH、HClO、H2S | HF |
| C | 复分解反应、电解反应、放热反应、离子反应 | 焰色反应 |
| D | (NH4)2SO4、NH4Cl、NH4NO3、NH3·H2O | NH4HCO3 |
(1)A中分类标准是______________________________________________,H2SO3________(填“是”或“否”)可归为此类。
(2)B中分类标准是_________________________________________________,HF________(填“是”或“否”)可归为此类。
(3)C中分类标准是__________________,焰色反应属于________变化。
(4)D中分类标准是__________________,NH4HCO3________(填“是”或“否”)可归为此类。
科目:高中化学 来源: 题型:
氢气是清洁的能源,也是重要的化工原料。
(1)以H2为原料制取氨气进而合成CO(NH2)2的反应如下:
N2(g)+3H2(g)=2NH3(g) △H=—92.40 kJ·mol-1
2NH3(g)+CO2(g)=NH2CO2NH4(s) △H=—159.47 kJ·mol-1
NH2CO2NH4(s)=CO(NH2)2(s)+H2O (l) △H=+72.49 kJ·mol-1
则N2(g)、H2(g)与CO2(g)反应生成CO(NH2)2(s)和H2O(l)的热化学方程式为 ▲ 。
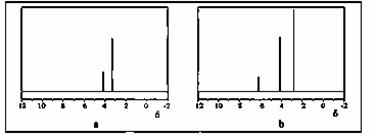
(2)用丙烷和水为原料在电催化下制氢气,同时得到一种含有三元环的环氧化合物A,该反应的化学方程式为 ▲ 。
该反应也可生成A的同分异构体——另一种环氧化合物B,B的核磁共振氢谱为
下图中的 ▲ (填“a”或“b”)。
(3)已知叠氮酸(HN3)不稳定,同时也能与活泼金属反应,反应方程式为:
2HN3=3N2↑+H2↑
2HN3+Zn=Zn(N3)2+H2↑
2 mol HN3与一定量Zn完全反应,在标准状况下生成67.2 L气体,其中N2的物质的量为 ▲ 。
(4)已知H2S高温热分解制H2的反应为:
H2S(g) H2(g)+1/2S2(g)
H2(g)+1/2S2(g)
在恒容密闭容器中,控制不同温度进行H2S的分解实验:
 以H2S的起始浓度均为c mol·L-1测定H2S的转化率,结果如右下图所示。图中
以H2S的起始浓度均为c mol·L-1测定H2S的转化率,结果如右下图所示。图中
a为H2S的平衡转化率与温度关系
曲线,b曲线表示不同温度下反应
经过相同时间且未达到化学平衡时
H2S的转化率。
若985℃时,反应经t min达到平衡,
此时H2S的转化率为40%,则反应
速率v(H2)= ▲ (用含c、t的代
数式表示)。
 请说明随温度的升高,曲线b向曲线a逼近的原因: ▲ 。
请说明随温度的升高,曲线b向曲线a逼近的原因: ▲ 。
(5)用惰性电极电解煤浆液的方法制H2的反应为:
C(s)+2H2O(l)=CO2(g)+2H2(g)
现将一定量的1 mol·L-1 H2SO4溶液和适量煤
粉充分混合,制成含碳量为0.02 g·mL-1~0.12
g·mL-1的煤浆液,置于右图所示装置中进行电
解(两电极均为惰性电极)。则A极的电极
反应式为 ▲ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
如图是198 K时N2与H2反应过程中能量变化的曲线图,下列叙述正确的是 ( )
 A.该反应的热化学方程式为N2+3H2
A.该反应的热化学方程式为N2+3H2 2NH3 ΔH=-92 kJ·mol-1
2NH3 ΔH=-92 kJ·mol-1
B.a曲线是加入催化剂时的能量变化曲线
C.加入催化剂,该化学反应的反应热改变
D.升高温度,反应速率加快
查看答案和解析>>
科目:高中化学 来源: 题型:
医药上有广泛的用途,其部分生产流程如图所示。
FeCl3·6H2O FeOOH
FeOOH 纳米四氧化三铁
纳米四氧化三铁
下列有关叙述不正确的是 ( )。
A.纳米四氧化三铁可分散在水中,其与FeCl3溶液中分散质的直径相当
B.纳米四氧化三铁具有磁性,可作为药物载体用于治疗疾病
C.在反应①中环丙胺的作用可促进氯化铁水解
D.反应②的化学方程式是6FeOOH+CO===2Fe3O4+3H2O+CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
药物贝诺酯可由乙酰水杨酸和对-乙酰氨基酚在一定条件下反应制得:

有关上述反应物和产物的叙述不正确的是( )
A.上述三种有机物中共有四种含氧官能团
B.贝诺酯分子中有9种不同化学环境的氢原子
C.贝诺酯与足量NaOH(aq)共热,最多消耗NaOH 4mol
D.可用FeCl3(aq) 区别乙酰水杨酸和对-乙酰氨基酚
查看答案和解析>>
科目:高中化学 来源: 题型:
用标准盐酸滴定未知浓度的NaOH溶液,下列各操作中,不会引起实验误差的是
A.用蒸馏水洗净滴定管后,装入标准盐酸进行滴定
B.用蒸馏水洗净锥形瓶后,再用NaOH溶液润洗,然后装入一定体积的NaOH溶液
C.用酚酞作指示剂时,滴至溶液从红色变成无色即视为滴定终点
D.用碱式滴定管取10.00mLNaOH溶液放入洗净的锥形瓶中,加入适量蒸馏水后,再进行滴定
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)某学生欲用11.9 mol·L-1的浓盐酸和蒸馏水配制500 mL物质的量浓度为0.400 mol·L-1的稀盐酸。 该学生需要量取________mL浓盐酸进行配制。(保留小数点后1位)
(2)容量瓶是配制溶液的必需仪器。下列关于容量瓶及其使用方法的叙述,错误的是
①是配制一定物质的量浓度的溶液的专用仪器
②使用前要先检查容量瓶是否漏液
③容量瓶可以用来加热
④不能用容量瓶长期贮存配制好的溶液
⑤可以用500mL容量瓶配制250mL溶液
⑥容量瓶上标有的是温度 、容量 、刻度线
a.① ③ b.① ④ c.③ ⑤ d.⑤ ⑥
(3)① 该同学用配制的0.400 mol·L-1的盐酸,中和含0.4 g NaOH的NaOH溶液,则该同学需取________mL盐酸。
② 假设该同学用新配制的盐酸中和含0.4 g NaOH的NaOH溶液,发现比①中所求体积偏小,则可能的原因是________。
a.浓盐酸挥发,浓度不足
b.配制溶液时,未洗涤烧杯
c.配制溶液时,俯视容量瓶刻度线
d.加水时超过刻度线,用胶头滴管吸出
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com